Décrits pour la première fois en 1773 par le zoologiste allemand Johann August Ephraim Goeze, les tardigrades sont des animaux extrêmophiles dépassant tout juste les 1 mm en moyenne. Leur particularité ? Ils résistent à de nombreuses conditions environnementales extrêmes, comme les hautes et basses températures, les hautes pressions, le vide, les radiations ou encore la famine. Pour mieux comprendre le secret de cette résistance spectaculaire, des chercheurs espagnols ont effectué une simulation complète des mécanismes biomoléculaires mis en jeu afin de déterminer comment la résistance des tardigrades émerge au niveau atomique.
Les tardigrades sont des animaux spectaculaires sous tous les aspects. Soumis à un stress environnemental tel que la déshydratation ou des températures extrêmes, ils se rétractent dans un état dans lequel leur métabolisme s’arrête pratiquement. Dans cet état, ils peuvent survivre sans eau pendant des décennies, tolérer des doses élevées de rayons gamma et X et survivre à des températures de -272 °C à 150 °C. Ils ont également passé 10 jours dans le vide de l’espace dans le cadre d’une expérience dédiée.
« Dsup »: une protéine de protection de l’ADN flexible, ajustable et adaptable en fonction du stress
Chez la plupart des autres organismes, ces types de stress détruisent l’ADN des cellules, mais les tardigrades ont une protéine suppresseuse de dommages (Dsup) qui protègent en quelque sorte l’ADN. Marina Mínguez-Toral et ses collègues du Centre de biotechnologie végétale et de génomique de Madrid ont effectué une simulation de l’interaction entre Dsup et l’ADN, qui éclaire un peu plus sur ces mécanismes. Les résultats ont été publiés dans la revue Scientific reports.
L’équipe a modélisé un système de deux molécules Dsup et d’ADN, comprenant plus de 750’000 atomes, ce qui a nécessité « des jours et des jours » de traitement par un supercalculateur. « Les équations du mouvement doivent être résolues pour chacun de ces atomes 50 millions de fois pour obtenir une simulation d’une durée de 100 nanosecondes », explique Mínguez-Toral. La modélisation par les chercheurs de tous les atomes de la protéine et de toutes leurs interactions électrostatiques montre que la protéine est « intrinsèquement désordonnée » et très flexible, et semble capable d’ajuster sa structure pour épouser précisément la forme de l’ADN.
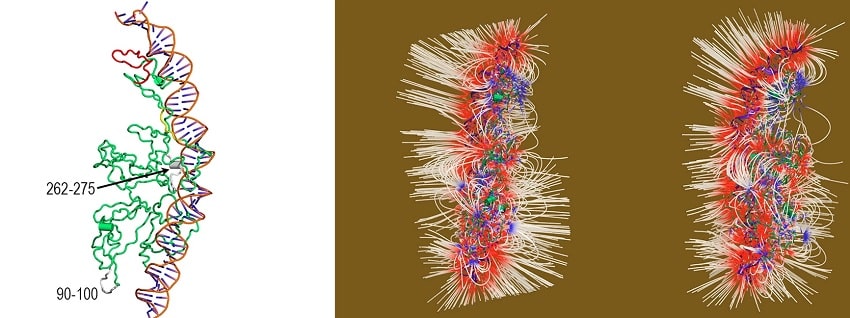
« Notre étude révèle que les effets électriques sous-jacents aux attractions de charge positive-négative déterminent la dynamique des changements structurels de Dsup dans son interaction avec l’ADN. Nous pensons que ce blindage électrique est primordial pour protéger l’ADN des radiations », indique Mínguez-Toral.
Sur le même sujet : Comment les tardigrades survivent-ils aux environnements extrêmes ?
Du cancer au voyage dans l’espace, un mécanisme de protection potentiellement utile pour l’Homme
Déterminer précisément comment les tardigrades tolèrent de tels extrêmes pourrait être utile de plusieurs manières. « À l’heure actuelle, les principales applications sur lesquelles nous travaillons activement sont la stabilisation des produits pharmaceutiques et l’ingénierie de plantes cultivées tolérantes au stress », explique Thomas Boothby, qui travaille avec les tardigrades à l’Université du Wyoming.
D’autres possibilités incluent le traitement du cancer ainsi que des applications futuristes telles que l’hibernation humaine et les voyages dans l’espace — les personnes se rendant sur Mars pourraient être modifiées pour être plus résistantes aux radiations, par exemple. En laboratoire, des cellules rénales humaines ont été génétiquement modifiées pour exprimer la Dsup des tardigrades, et ces cellules ont montré une réduction de 40 à 50 pour cent des dommages à l’ADN causés par les rayons X.
La prochaine étape serait de modifier toutes les cellules d’un autre organisme, et les cobayes de laboratoire tels que le ver rond et la mouche des fruits semblent être de bons candidats. Cependant, Mínguez-Toral et son collègue Luis Pacios soulignent que nous ne savons pas pourquoi Dsup a évolué, et nous devons le comprendre avant de commencer à penser à modifier des organismes entiers.