Les maladies chroniques sont de loin les premières causes de mortalité à travers le monde, avec pas moins de 41 millions de décès chaque année. Elles ont un impact majeur sur la qualité de vie, engendrant des incapacités et des difficultés personnelles, familiales et socioprofessionnelles importantes. Récemment, des chercheurs suédois du Karolinska Institutet ont démontré l’effet de la neurostimulation du nerf vague dans la réduction de l’inflammation chronique. Plus long nerf du corps, il est au cœur de la communication entre le cerveau et nos organes internes, le rendant stratégique dans de nombreuses thérapies. Cette découverte apporte de nouvelles preuves concernant les nombreux « pouvoirs » de ce nerf et donnent l’espoir de mettre un terme au fardeau de l’inflammation chronique pour les patients et le système de santé.
L’OMS (Organisation Mondiale de la Santé) définit les maladies chroniques comme des affections de longue durée qui, en règle générale, évoluent lentement et résultent d’une association de facteurs génétiques, physiologiques, environnementaux et comportementaux. En particulier, les maladies inflammatoires chroniques peuvent être la conséquence de maladies auto-immunes et regroupent notamment la polyarthrite rhumatoïde (inflammation des articulations), les maladies inflammatoires chroniques de l’intestin — comme la maladie de Crohn —, la spondylarthrite ankylosante (inflammation d’un ou plusieurs os), pour ne citer que quelques exemples.
Il faut préciser qu’en temps normal, la résolution de l’inflammation est un processus actif qui restaure l’homéostasie tissulaire et prévient le développement de maladies inflammatoires chroniques. Malheureusement, les mécanismes qui régulent la résolution de l’inflammation ne sont que partiellement compris, rendant extrêmement difficile la mise en place de thérapies soulageant les patients de manière efficace et durable.
Le nerf vague est le nerf principal du système nerveux autonome parasympathique. Outre ses fonctions végétatives, il a des propriétés anti-inflammatoires et analgésiques. En agissant sur le système immunitaire, il permet d’empêcher un emballement inflammatoire et pourrait donc potentiellement aider à résoudre l’inflammation chronique. C’est dans ce contexte que des chercheurs du Karolinska Institutet en Suède, démontrent comment la stimulation électrique de ce nerf spécifique peut favoriser la guérison d’une inflammation aiguë. Leur étude est publiée dans la revue PNAS.
Le nerf vague, lien stratégique entre cerveau et organes
Dans un premier temps, replaçons ce nerf dans le plan du corps. Il s’agit d’une paire de nerfs crâniens constituée à 80% de fibres nerveuses sensorielles qui transmettent les informations de nature chimique, mécanique et thermique, issues de nos organes internes jusqu’au cerveau. Les 20% de fibres restantes font le chemin inverse en véhiculant les « ordres » du cerveau vers nos organes.
Dans les années 1940, des physiologistes se lancent dans les premières expérimentations sur la stimulation électrique du nerf vague. Les travaux du neurophysiologiste américain Jacob Zabara sur des chats ont abouti, des décennies plus tard, à l’utilisation de cette technique contre l’épilepsie réfractaire. Depuis, les preuves de l’implication du nerf vague dans la plupart des mécanismes du corps se multiplient : il aide notamment à la récupération physiologique en favorisant le sommeil, le calme émotionnel, le bon fonctionnement digestif et immunitaire.
C’est ainsi que l’activité du nerf vague est à son plus haut niveau, lorsque nous sommes dans un état émotionnel positif et calme, maintenant notre rythme cardiaque, au repos, autour de 50-60 battements par minute. Sans lui, notre rythme cardiaque s’élèverait à 100-110 battements par minute au repos ! À l’inverse, en état de stress, l’activité du nerf vague est inhibée, il ne peut exercer ni son pouvoir anti-inflammatoire, ni son action calmante sur le rythme cardiaque. Une fois l’événement stressant surmonté, l’activité du nerf vague se rétablit, induisant la récupération physique et psychologique. Cependant, dans certains troubles émotionnels, comme la dépression ou l’anxiété, l’activité vagale s’effondre, tout comme lors de l’inflammation chronique.
Sans compter que l’état émotionnel et le stress sont fortement impliqués dans l’initiation et l’aggravation de certaines maladies inflammatoires chroniques de l’intestin, ainsi que de la polyarthrite rhumatoïde. Ces pathologies sont associées à des anomalies dans la communication nerveuse.
Une neurostimulation contre les maladies chroniques
Les scientifiques de la présente étude se sont basés sur des recherches antérieures menées par le groupe de Peder Olofsson au Karolinska Institutet et d’autres groupes de recherche ayant établi que la stimulation électrique du nerf vague peut réduire l’inflammation et rétablir une communication optimale ente le cerveau et les organes. Cette électrostimulation est en cours d’évaluation dans plusieurs maladies musculosquelettiques. Cependant, la façon dont les signaux nerveux régulent la résolution active de l’inflammation n’est toujours pas comprise.
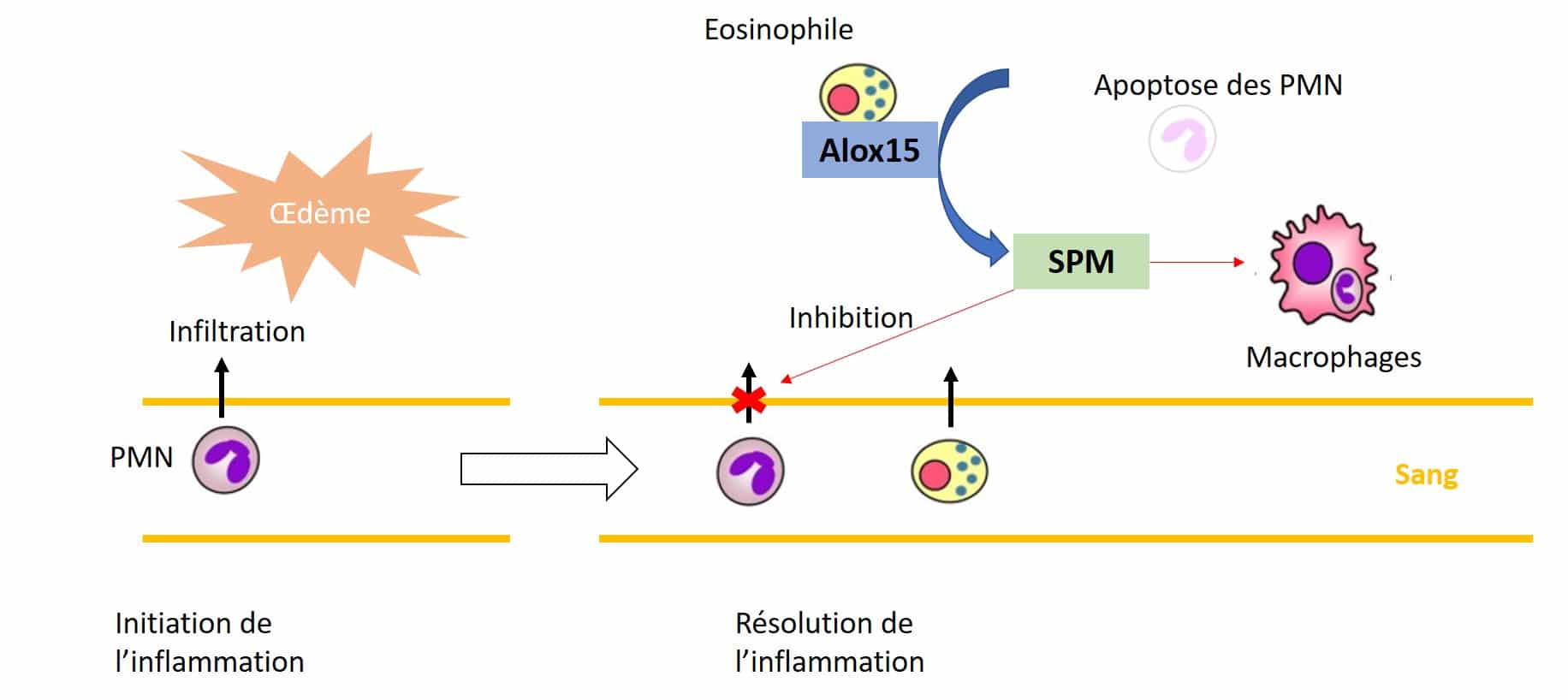
Effectivement, lors d’un processus inflammatoire normal, la phase d’initiation de l’inflammation aiguë est caractérisée par l’infiltration rapide de neutrophiles polymorphonucléaires (PMN) suivie de l’infiltration de monocytes, se transformant en macrophages, ainsi que par la formation d’œdèmes, en réponse à une blessure par exemple. Les PMN fournissent la première ligne de défense immunitaire en migrant vers les sites de blessure et en neutralisant les micro-organismes envahisseurs ou les matières nocives par phagocytose. Puis, des éosinophiles sont recrutés au niveau du site enflammé et produisent des médiateurs lipidiques anti-inflammatoires et pro-résolution spécialisés (SPM), via certaines enzymes (comme Alox15). Ces derniers bloquent l’infiltration des PMN, qui subissent alors une apoptose (mort cellulaire) et sont ingérés par des macrophages. Les chercheurs ont donc voulu comprendre comment intervient le nerf vague dans ce processus.
April S. Caravaca, l’une des auteurs de l’étude, déclare dans un communiqué de l’Université : « Nous avons maintenant étudié les effets des signaux entre les nerfs et les cellules immunitaires au niveau moléculaire. Une meilleure compréhension de ces mécanismes permettra des applications plus précises qui exploitent le système nerveux pour réguler l’inflammation ».
Par ailleurs, cette neurostimulation peut être invasive, avec une électrode placée autour du nerf vague cervical et reliée à un générateur implanté en sous-cutané, ou non invasive lorsque la stimulation d’une branche du nerf vague (auriculaire ou cervicale) se fait en percutané. Elle ne peut donc pas être prescrite sans que des assurances d’efficacité ne soit rapportées, de manière certaine, autant que faire se peut.
Un mécanisme d’action précis pour le nerf vague
Pour étudier le mécanisme sous-jacent à cette action nerveuse, les chercheurs ont soumis des souris soit à une stimulation électrique du nerf vague invasive, soit à une chirurgie factice au niveau cervical, suivie d’une péritonite induite par le zymosan (composé chimique), provoquant dans les deux cas une inflammation sévère. Par suite, ils ont étudié les taux de médiateurs présents chez les souris et le temps de résolution de l’inflammation. Ils ont constaté un nombre plus important de médiateurs de pro-résolution spécialisés (SPM) pour les souris ayant reçu la stimulation électrique.
En termes simples, les chercheurs ont montré que la stimulation électrique du nerf vague, lors d’une inflammation, modifie l’équilibre entre les molécules inflammatoires et anti-inflammatoires spécialisées, ce qui favorise la guérison.
Une nuance est toutefois apportée. En effet, les scientifiques ont découvert que l’accélération de la résolution de l’inflammation par la neurostimulation était altérée chez les souris génétiquement déficientes, soit en Alox15 — enzyme clé dans la biosynthèse des SPM par les éosinophiles —, soit en une sous-unité du récepteur à l’acétylcholine — neuromédiateur entre certains synapses —, située sur les cellules immunitaires. Ensemble, ces observations démontrent que bien que le nerf vague contrôle la résolution de l’inflammation, ce mécanisme se fait via la régulation cholinergique (liée à l’acétylcholine) du microenvironnement de l’inflammation et la biosynthèse des médiateurs de pro-résolution spécialisés.
Peder Olofsson conclut : « L’inflammation et sa résolution jouent un rôle clé dans un large éventail de maladies courantes, y compris les maladies auto-immunes et les maladies cardiovasculaires. Nos découvertes fournissent des informations sur la façon dont le système nerveux peut accélérer la résolution de l’inflammation en activant des voies de signalisation définies ».
Les chercheurs continuent d’étudier plus en détail comment les nerfs interviennent dans la guérison de l’inflammation. En effet, le nerf vague n’est pas seul : tout un réseau de nerfs régule l’inflammation au niveau moléculaire. Les auteurs espèrent que les conclusions de leurs recherches fourniront une meilleure compréhension du phénomène inflammatoire pathologique et contribueront à des traitements plus efficaces pour de nombreuses maladies inflammatoires.