Depuis la mise au point de l’outil d’édition génétique CRISPR, de nombreux domaines, de la biologie à la médecine, ont pu profiter des possibilités de modifications génétiques offertes par cette méthode. Le génie génétique a déjà apporté des solutions thérapeutiques à diverses pathologies et c’est aujourd’hui le tour de deux maladies génétiques relativement répandues : la bêta-thalassémie et la drépanocytose. En effet, des patients souffrant de ces maladies ont été traités par CRISPR et n’ont aujourd’hui plus besoin de transfusions sanguines.
Deux personnes atteintes de bêta-thalassémie et une de drépanocytose n’ont plus besoin de transfusions sanguines, qui sont normalement utilisées pour traiter les formes graves de ces maladies héréditaires, après que leurs cellules souches de la moelle osseuse ont été génétiquement modifiées avec CRISPR. Le résultat de cet essai en cours, qui est le premier à utiliser CRISPR pour traiter les troubles génétiques héréditaires, a été annoncé lors d’une réunion virtuelle de l’Association européenne d’hématologie.
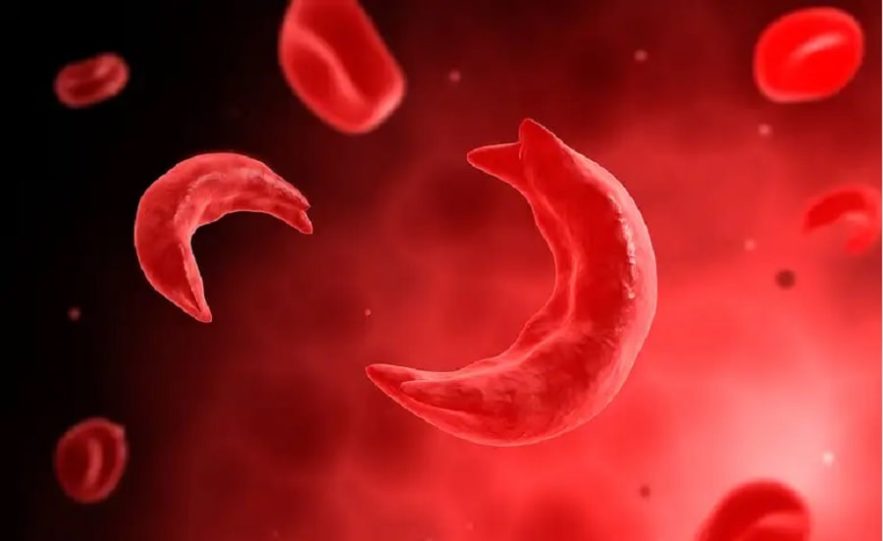
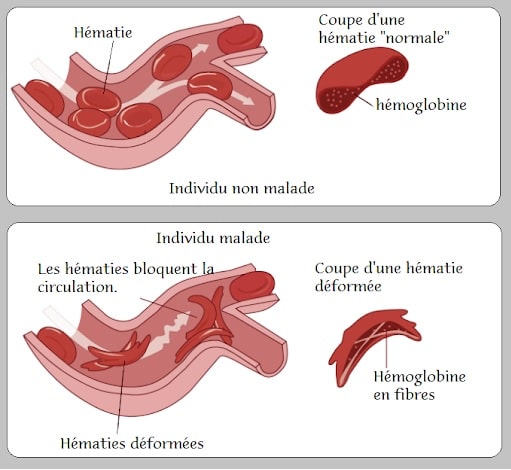
« Les résultats préliminaires démontrent, en substance, un remède fonctionnel pour les patients atteints de bêta-thalassémie et de drépanocytose », déclare Haydar Frangoul du Sarah Cannon Research Institute à Nashville. La bêta-thalassémie et la drépanocytose sont des pathologies causées par des mutations qui affectent l’hémoglobine, la protéine qui transporte l’oxygène dans les globules rouges. Les personnes atteintes de formes sévères nécessitent des transfusions sanguines régulières.
Relancer la production d’hémoglobine fœtale grâce à CRISPR
Cependant, quelques personnes atteintes de ces mutations ne présentent aucun symptôme, car elles continuent de produire de l’hémoglobine fœtale à l’âge adulte. Normalement, l’hémoglobine fœtale cesse d’être produite peu de temps après la naissance. Cette découverte a inspiré le développement de traitements basés sur la stimulation de l’hémoglobine fœtale. Dans cet essai, dirigé par les sociétés collaboratrices CRISPR Therapeutics et Vertex, les cellules souches de la moelle osseuse sont retirées des personnes et le gène qui inhibe la production d’hémoglobine fœtale est désactivé avec CRISPR.
Sur le même sujet : Cancer : un essai clinique suggère que l’édition génétique CRISPR pourrait être un traitement viable
Les cellules de moelle osseuse restantes sont tuées par chimiothérapie, puis remplacées par des cellules modifiées. Ceci est fait pour s’assurer que de nouvelles cellules sanguines sont produites par les cellules souches modifiées, mais la chimiothérapie peut avoir des effets secondaires graves, y compris l’infertilité. Les deux premiers patients atteints de bêta-thalassémie n’ont plus besoin de transfusions sanguines depuis leur traitement il y a 15 et 5 mois. Le patient atteint de drépanocytose non plus, neuf mois après le traitement.
Une méthode sûre mais une surveillance potentielle nécessaire
Les résultats sont excellents, affirme Marina Cavazzana de l’hôpital Necker-Enfants Malades à Paris, dont l’équipe a traité un garçon de 13 ans atteint de drépanocytose en utilisant une approche différente. Bien que les trois patients aient éprouvé des effets indésirables dus à la chimiothérapie, l’édition du gène CRISPR semble sûre.
Cependant, les patients peuvent avoir besoin d’être surveillés pour le reste de leur vie pour être sûr qu’ils n’ont aucun effet indésirable. Au total, cinq personnes ont été traitées. L’essai avait été suspendu en raison de la pandémie de coronavirus, mais a maintenant repris.