Les molécules d’ADN sont généralement formées de deux brins enroulés l’un autour de l’autre. Cette structure en double hélice, commune à toutes les espèces, a été mise en évidence en 1953 par les biologistes James Watson et Francis Crick. Il y a 7 ans, de l’ADN à quadruple hélice a été détecté dans les cellules humaines, mais la technique utilisée nécessitait de détruire lesdites cellules, de sorte que l’observation de ce type d’ADN in vivo n’a jamais pu être réalisée. Des chercheurs britanniques présentent aujourd’hui une nouvelle technique pour visualiser cet ADN atypique et mieux comprendre son rôle biologique.
Jusqu’à présent, aucune structure d’ADN autre que la célèbre double hélice n’avait été observée dans des cellules vivantes. Mais cette équipe de scientifiques a conçu un nouveau type de marqueur fluorescent, capable de se fixer à l’ADN à quadruple hélice. La substance permet ainsi de visualiser pour la première fois comment cette structure se forme et surtout, quel rôle elle joue.
Une structure liée aux cellules cancéreuses
La mise en évidence d’ADN à quadruple hélice dans les cellules humaines date de 2013. Depuis, il fait l’objet de nombreuses études, car il a rapidement été associé au développement de cancers et de maladies rares. Cet ADN est composé non pas de deux, mais de quatre brins s’enroulant les uns autour des autres. Il se forme par repliement d’ADN « standard », lorsqu’il est riche en guanine (notée G), l’une des quatre bases nucléiques qui le constituent. En s’assemblant entre elles, ces bases G forment une structure à 4 brins, très riche en guanine ; d’où le nom de « quadruplexes G4 ».
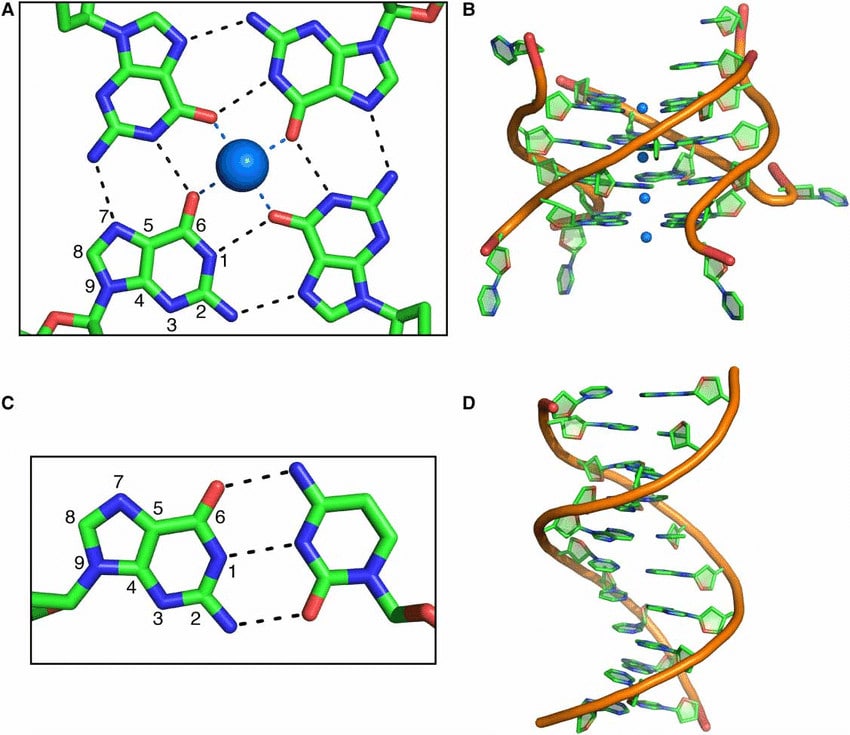
L’équipe de chercheurs, menée par le Dr Marco Di Antonio du département de chimie de l’Université de Cambridge, a ainsi prouvé que les quadruplexes G4 existent bel et bien dans nos cellules et sont créés par des processus cellulaires standards. Cette découverte remet en question toute la biologie de l’ADN et pourrait même être une piste vers de nouveaux diagnostics et traitements de certaines maladies, comme le cancer. Mais pour parvenir à cet objectif, il était indispensable de parvenir à observer ces molécules dans leur environnement.
En 2016, lors de précédentes expérimentations, cette équipe de Cambridge avait entrepris d’observer les G4 en conditions réelles via des anticorps capables de reconnaître et de se fixer à cet ADN spécifique. Toutefois, la technique nécessitait d’utiliser des concentrations très élevées de ces molécules « sondes ». De ce fait, ces dernières pouvaient potentiellement perturber l’ADN et favoriser la formation involontaire de G4. Or, les chercheurs souhaitaient détecter les G4 issus d’une formation spontanée et naturelle.
L’enjeu était donc de trouver le moyen de créer des sondes capables d’observer ces éléments in vivo, sans qu’elles puissent interagir d’une façon ou d’une autre avec leur cible. La méthode d’observation par marqueur fluorescent utilisée dans cette nouvelle étude a été développée par le Dr Aleks Ponjavic, de l’Université de Leeds. Elle permet d’observer par microscopie des molécules-sondes à des concentrations 1000 fois plus faibles que celles utilisées auparavant !
Inhiber la formation des G4 : une piste pour soigner le cancer
En pratique, la sonde conçue par l’équipe se fixe aux quadruplexes d’ADN pendant quelques millisecondes uniquement, sans affecter sa stabilité ; ce laps de temps est suffisant pour étudier le comportement des G4 dans leur environnement naturel, sans qu’ils ne soient soumis à aucune influence externe. La sonde est constituée d’une molécule fluorescente particulièrement brillante, ce qui permet d’en limiter la quantité ; elle est en outre conçue pour adhérer aisément aux G4.
Les chercheurs ont notamment constaté que les G4 se forment et se dissipent très rapidement dans les cellules. Par conséquent, ils pensent qu’ils n’y apparaissent que pour remplir une fonction bien spécifique ; s’ils persistaient plus longtemps, ils pourraient potentiellement nuire aux autres processus cellulaires standards. Ils ont également noté que la formation de G4 dans les cellules vivantes dépendait du cycle cellulaire ; elle semble notamment perturbée par l’inhibition chimique de la transcription et de la réplication.
Sur le même sujet : Tests d’ADN en ligne ; quelles informations nous fournissent-ils ? Sont-ils fiables ?
En suivant en temps réel les G4 dans les cellules, ils ont remarqué — sans grand étonnement — que cette structure particulière semble être bien plus répandue dans les cellules cancéreuses. Un constat qui corrobore plusieurs études antérieures révélant que les quadruplexes G4 sont intimement liés à l’instabilité du génome et impliqués dans le cancer, ou d’autres maladies neurodégénératives ou infectieuses.
On sait depuis peu que les G4 interviennent dans plusieurs processus biologiques clés, comme la réplication et la transcription d’ADN, ou la traduction de l’ARN (processus permettant la synthèse des protéines). L’équipe affirme qu’il est désormais possible de suivre un G4 tout au long de sa vie, afin d’examiner son rôle précis dans l’expression des gènes, notamment ceux liés au cancer. Une fois ces informations connues, elles pourraient déboucher vers le développement de nouvelles thérapies prenant ces G4 pour cibles. Exploiter ainsi les faiblesses des cellules cancéreuses constitue en outre une approche moins risquée pour les cellules saines, et réduirait les effets secondaires potentiels du traitement.