L’inconvénient le plus évident des énergies renouvelables telles que l’énergie solaire et éolienne est que leur production manque de continuité. Une solution consiste à convertir l’électricité produite par ces systèmes en molécules de carburant organiques telles que le méthane et le monoxyde de carbone. Mais les carburants à base de carbone sont finalement transformés en dioxyde de carbone après utilisation. Et cela représente un problème majeur pour l’environnement.
C’est pourquoi les scientifiques ont cherché des alternatives qui ne libèrent pas de gaz à effet de serre. L’ammoniac est apparu comme un candidat potentiel.
Les molécules produites grâce à l’électricité générée par les éoliennes ou panneaux solaires doivent pouvoir être stockées et transportées librement vers des sites de consommation. Les chercheurs devaient donc trouver une solution répondant à ce critère, mais qui dégagerait moins ou voire pas du tout de dioxyde de carbone après utilisation.
Il se trouve que l’ammoniac n’est pas constitué de carbone. En effet, sa combustion avec de l’oxygène libère de l’azote gazeux et de l’eau. Une grande quantité d’énergie est ainsi libérée, et sans dégagement de dioxyde de carbone.
Sujet similaire :
Une nouvelle méthode pour générer de l’oxygène et de l’hydrogène dans l’espace à partir d’eau
De récentes études ont prouvé qu’il peut être produit de manière douce et respectueuse de l’environnement, dans une pile à combustible fonctionnant à l’énergie solaire et utilisant uniquement de l’eau et de l’air comme matières premières. Dans le prototype présenté, les cations d’hydrogène produits par l’électrolyse de l’eau réagissent avec les molécules d’azote extraites de l’air. La réaction est lente mais efficace, et nécessite une pression atmosphérique ainsi qu’une température ambiante.
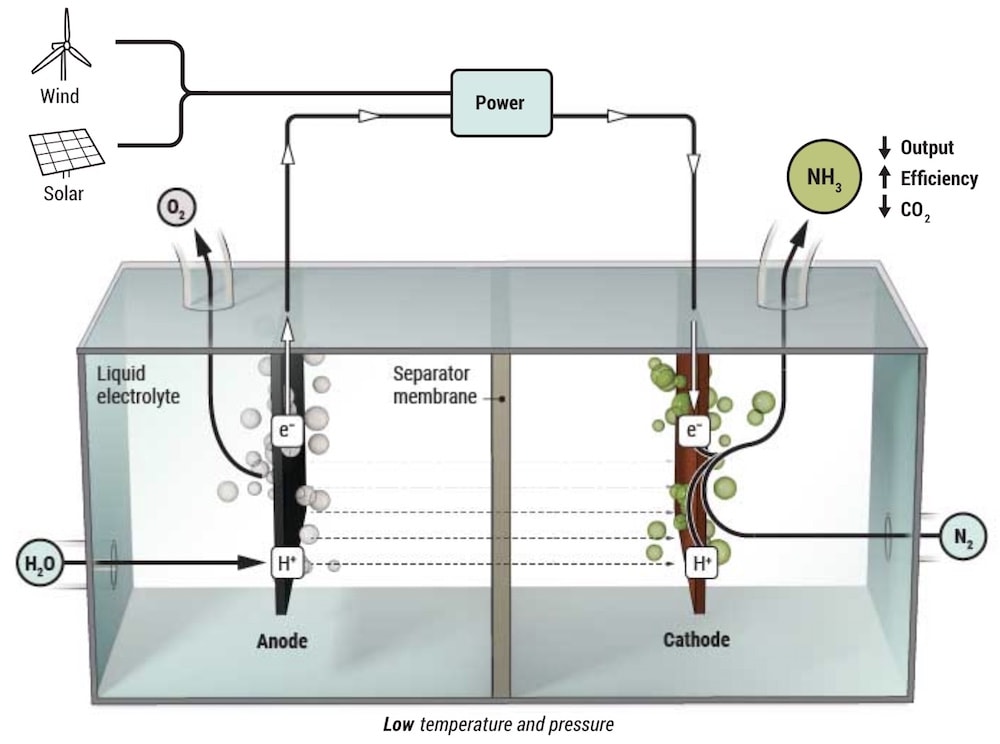
Mais à l’heure actuelle, les rendements sont modestes. À température et pression ambiantes, les réactions des piles à combustible ont généralement des rendements compris entre 1% et 15%, et le débit (vitesse de la réaction) est faible. Mais Douglas MacFarlane, chimiste à l’Université de Monash à Melbourne (Australie), a trouvé un moyen de stimuler l’efficacité en changeant l’électrolyte.
Dans l’électrolyte à base d’eau que de nombreux groupes utilisent, les molécules d’eau réagissent parfois avec des électrons au niveau de la cathode, en « volant » des électrons qui autrement conduiraient à la formation d’ammoniac. « Nous « luttons » constamment pour pas que les électrons conduisent à la formation d’hydrogène », explique MacFarlane.
Pour contrer ce problème, le chimiste a opté pour ce qu’on appelle un électrolyte liquide ionique. Cette approche permet à davantage de diazote (N2) et à moins d’eau de se « bloquer » près des catalyseurs sur la cathode, ce qui stimule la production d’ammoniac. En conséquence, l’efficacité de la pile à combustible est passée de moins de 15% à 60%.
Plus récemment, le rendement a encore été amélioré pour atteindre les 70%, selon MacFarlane. Mais cela n’a pas été possible sans compromis : le liquide ionique dans la pile à combustible développée est très visqueux, 10 fois plus que l’eau. Les protons doivent se frayer un chemin jusqu’à la cathode, ce qui ralentit le taux de production d’ammoniac. « Cela représente un véritable challenge pour nous » déclare MacFarlane.
Pour accélérer les choses, MacFarlane et ses collègues ont effectué plusieurs tests avec différents liquides ioniques. Dans une étude publiée en avril dans le ACS Energy Letters, ils rapportent avoir inventé un liquide riche en fluor, qui aide les protons à se déplacer plus facilement au sein du milieu et qui accélère la production d’ammoniac d’un facteur 10. Mais le taux de production doit encore être augmenté de plusieurs ordres de grandeur pour atteindre les objectifs fixés pour le domaine par le Département américain de l’énergie (DOE).
Près de l’Université Monash, Sarb Giddey et ses collègues des bureaux de CSIRO Energy à Clayton, fabriquent de l’ammoniac avec leur « réacteur à membrane ». Le système fonctionne avec des températures élevées et des pressions faibles qui, par rapport à la technique de MacFarlane, augmentent le débit tout en diminuant le rendement.
La conception de réacteurs nécessite une paire de tubes métalliques concentriques longs, chauffés à 450 °C. Dans l’espace étroit entre les tubes s’écoule du H2, qui pourrait être produit par un électrolyseur solaire ou éolien.
Les catalyseurs qui tapissent la paroi interne divisent les molécules de dihydrogène (H2) en atomes d’hydrogène individuels (H), qui exercent alors des pressions modestes à travers le réseau atomique depuis la paroi du tube jusqu’à son noyau creux, où attendent des molécules de N2 injectées dans le tube.
Un métal catalytiquement actif tel que le palladium tapisse la surface interne, séparant le N2 et coaxant l’hydrogène et l’azote pour se combiner en ammoniac. Le processus est ici beaucoup plus rapide que celui de la cellule de MacFarlane. Jusqu’à présent, seulement une petite fraction du H2 réagit – une autre problématique concernant l’efficacité du réacteur.

D’autres approches sont en cours de développement. À la Colorado School of Mines située à Golden (États-Unis), des chercheurs dirigés par Ryan O’Hayre développent des piles à combustible inversées de la taille d’un bouton de veste.
Fabriquées à partir de céramiques pour résister à des températures de fonctionnement élevées, les cellules peuvent synthétiser de l’ammoniac à des vitesses record – environ 500 fois plus rapidement que la pile à combustible de MacFarlane.
Comme les réacteurs à membrane de Giddey, les piles à combustible en céramique privilégient le débit de production en dépit du rendement. Pourtant, O’Hayre explique qu’ils est encore nécessaire d’améliorer les taux de production d’un facteur 70 pour atteindre les objectifs définis par le DOE. « Nous avons énormément d’idées », s’enthousiasme O’Hayre.
Les différentes équipes de recherche doivent donc maintenant travailler sur leurs systèmes respectifs afin d’en améliorer le rendement et le débit de production, peut-être en combinant leurs efforts et technologies.
Convertir l’hydrogène en ammoniac dans l’unique but de le convertir à nouveau en hydrogène peut sembler étrange. Mais l’hydrogène est difficile à transporter : il doit être liquéfié en le refroidissant à des températures inférieures à -253 °C, en consommant jusqu’à un tiers de son contenu énergétique. Par contre, l’ammoniac se liquéfie à -10 °C, et nécessite peu de pression.
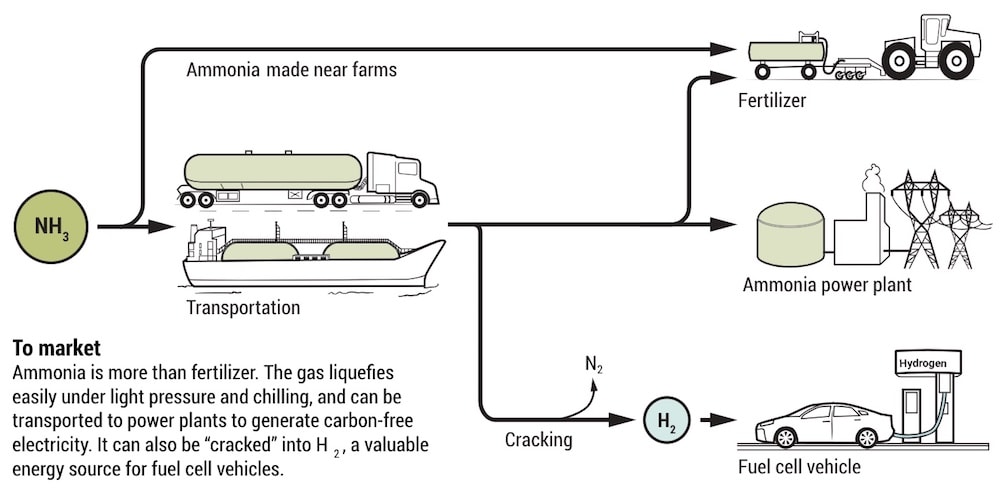
La perte énergétique résultant de la conversion d’hydrogène en ammoniac puis à nouveau en hydrogène, est cependant à peu près la même que celle résultant du refroidissement de l’hydrogène, précise Michael Dolan, chimiste à CSIRO Energy à Brisbane. Mais il existe déjà beaucoup plus d’infrastructures pour la manipulation et le transport de l’ammoniac, c’est surtout pour cela qu’il s’agit du pari le plus sûr.
Une vidéo expliquant très bien le principe :



 L’électron est une particule élémentaire qui, avec les protons et
les neutrons, constitue les atomes. C’est donc l’un des composants
principaux de la matière baryonique. À ce titre, il revêt... [...]
L’électron est une particule élémentaire qui, avec les protons et
les neutrons, constitue les atomes. C’est donc l’un des composants
principaux de la matière baryonique. À ce titre, il revêt... [...]