En France, on dénombre chaque année plus de 140’000 nouveaux cas d’accidents vasculaires cérébraux (AVC), soit un toutes les quatre minutes. Dans 40% des cas, l’accident entraîne des séquelles importantes, au niveau moteur, cognitif et sensitif ; c’est la première cause de handicap physique acquis chez l’adulte. Des chercheurs suédois se sont intéressés aux lésions cérébrales occasionnées par un AVC et sont ainsi parvenus à les réparer chez le rat. Un espoir pour toutes les futures victimes de cet accident vasculaire qui reste difficile à anticiper…
Un accident vasculaire cérébral (AVC) résulte de l’interruption de la circulation sanguine dans le cerveau, suite à la rupture d’un vaisseau sanguin ou à la présence d’un caillot. Le cerveau est alors momentanément privé d’oxygène et de nutriments, ce qui peut avoir des conséquences dramatiques ; celles-ci dépendent notamment de la partie du cerveau atteinte et de la durée pendant laquelle le cerveau n’est plus irrigué. S’ensuit généralement une longue période de rééducation, qui ne garantit pas toujours une récupération totale des capacités.
Une greffe de neurones pour rétablir les connexions
La transplantation de cellules souches a déjà été proposée comme une nouvelle stratégie thérapeutique pour favoriser la récupération. Dans cette nouvelle étude, des experts montrent que dans le cas des rats, de nouvelles connexions peuvent même s’établir dans le cerveau et restaurer certaines fonctions. Ainsi, il sera peut-être un jour possible de remplacer les cellules cérébrales endommagées par des cellules souches et ainsi, d’éliminer les séquelles inhérentes aux AVC.
Une équipe de neurologues de l’Université de Lund a en effet réussi à restaurer la mobilité et la sensation du toucher chez des rats ayant subi un AVC. Pour ce faire, ils ont reprogrammé des cellules de peau humaine de manière à ce qu’elles deviennent des cellules nerveuses, qu’ils ont ensuite transplantées dans le cerveau des rongeurs. Leurs résultats très encourageants ont été publiés dans la revue Proceedings of the National Academy of Sciences.
Des études antérieures menées par l’équipe avaient déjà démontré qu’il était possible de transplanter ainsi des cellules neuronales dérivées de cellules souches humaines dans le cerveau des rats atteints d’un AVC. Il s’agit de la technique des « cellules souches pluripotentes induites », ou iPS (pour induced pluripotent stem cells), qui consiste à reprogrammer génétiquement n’importe quelle cellule pour la rendre pluripotente. Une technique utilisée aujourd’hui dans de nombreuses applications biomédicales.
Toutefois, les spécialistes n’étaient pas encore parvenus à déterminer si ces cellules étaient capables de rétablir des connexions neuronales de manière à ce que le rat retrouve ses facultés motrices et sensitives initiales. C’est désormais chose faite. « Six mois après la transplantation, nous avons pu voir comment les nouvelles cellules avaient réparé les dommages causés par un accident vasculaire cérébral dans le cerveau des rats », explique le professeur Zaal Kokaia, l’un des auteurs de l’étude.
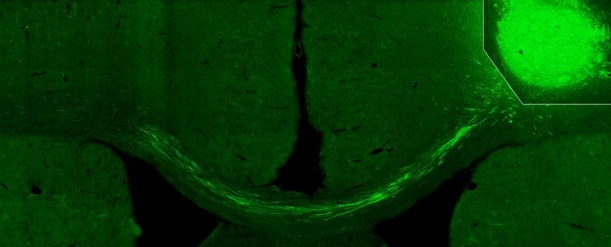
Concrètement, les projections axonales des cellules transplantées se sont développées dans une zone du cerveau, où aucune cellule n’avait été transplantée. Ces projections ont été complètement intégrées, tant d’un point de vue morphologique que fonctionnel, dans le réseau neuronal cérébral du rat. C’est une première pour les chercheurs à l’origine de l’étude, particulièrement surpris par ce résultat.
Une piste pour l’Homme… mais pas pour demain
À l’aide d’un traçage transsynaptique, les neurologues ont mis en évidence le fait que les neurones hôtes du cortex cérébral du rat recevaient des entrées monosynaptiques issues des cellules neuronales greffées. Ils ont également mis en évidence, par microscopie électronique, la myélinisation des axones dérivés du greffon dans le corps calleux – la zone qui interconnecte les deux hémisphères cérébraux ; leurs terminaisons formaient des synapses excitatrices sur les neurones corticaux hôtes. Enfin, un test sensorimoteur a permis à l’équipe de montrer que l’asymétrie induite par un AVC peut finalement s’inverser par transplantation ; leurs données indiquent que l’activité dans les neurones greffés est clairement impliquée dans le maintien d’une fonction motrice normale.
Sur le même sujet : Un lien entre sommeil excessif et augmentation du risque d’AVC : jusqu’à 85% !
À présent, les experts souhaitent aller plus loin dans leurs recherches pour bien comprendre comment les cellules transplantées affectent le cerveau. « Nous voulons également examiner de plus près comment une greffe affecte les fonctions intellectuelles telles que la mémoire. De plus, nous étudierons les effets secondaires possibles », explique Zaal Kokaia. Il souligne en effet que la sécurité est ici extrêmement importante si ce type de transplantation cellulaire doit être utilisée cliniquement à l’avenir. Beaucoup reste à faire avant que la procédure ne puisse être considérée comme appropriée et sûre pour les patients humains.
En attendant, certains chercheurs explorent d’autres pistes, telles que les endozépines, des peptides naturellement produits par le cerveau, qui augmentent la plasticité synaptique. Chez la souris, ils améliorent la communication entre les neurones dans les zones en réparation après un AVC, à condition de débuter le traitement de façon précoce. D’autres cherchent à développer de nouvelles méthodes de rééducation pour permettre aux victimes d’AVC de retrouver plus rapidement leur autonomie, notamment grâce à des interfaces cerveau-machine.