Une nouvelle technique de bioimpression 3D à base de cellules souches pluripotentes induites humaines (hiPSC) permet d’effectuer des réparations cérébrales sur mesure. Imprimés sous forme de gouttelettes bicouches, les tissus obtenus imitent l’architecture des régions endommagées du cortex cérébral. Lors d’essais ex vivo sur des cerveaux murins, les implants se sont correctement connectés aux cellules neurales hôtes. À terme, ces tissus bioimprimés pourraient constituer une alternative prometteuse pour les patients souffrant de lésions cérébrales sévères.
Qu’elles soient causées par un traumatisme, un accident vasculaire cérébral, une intervention chirurgicale ou une pathologie (telle que l’épilepsie), les lésions cérébrales peuvent entraîner d’importantes altérations fonctionnelles, selon leur localisation et leur taille. Selon la sévérité, les séquelles vont des difficultés cognitives aux troubles du mouvement et de la communication. Les techniques de régénération tissulaire à base de hiPSC sont désormais explorées dans l’espoir de réparer ces lésions. Les implants basés sur ce type de cellules possèdent notamment l’avantage de minimiser les réponses immunitaires potentiellement délétères pour l’hôte, sans compter leur grande polyvalence en matière de différenciation.
Cependant, la capacité des implants obtenus à imiter l’architecture naturelle du cerveau représente un défi majeur. En effet, le cortex cérébral possède une structure complexe à 6 couches, chacune composée de neurones spécifiques. De la partie la plus externe à la plus interne, les couches 1 à 4 sont dites supérieures, tandis que les 2 autres sont dites profondes. La connexion intracorticale des circuits neuronaux entre ces strates assure un rôle essentiel dans les fonctions cognitives supérieures, chez les mammifères. Pour l’heure, aucun implant cellulaire ou à base d’organoïde n’est capable d’imiter correctement cette architecture multicouche, ce qui entrave l’efficacité des thérapies régénératives.
Dans le but de surmonter ce défi, des chercheurs de l’Université d’Oxford ont eu pour idée d’implanter des structures simplifiées ressemblant aux couches des régions corticales au niveau desquelles les lésions sont situées. « Plutôt que l’implantation de cellules ou d’organoïdes dissociés dérivés de hiPSC, dépourvus de contrôle structurel, nous supposons que l’implantation de tissus ressemblant à l’architecture cellulaire du tissu endommagé offrira des traitements plus efficaces », expliquent-ils dans leur rapport, publié dans la revue Nature Communications. Grâce à une nouvelle technique de bioimpression 3D qu’ils ont mis au point, les réparations des lésions sont faites sur mesure, selon leur gravité et leur emplacement dans le cortex, ainsi que selon diverses caractéristiques des patients.
Des implants sous forme de gouttelettes
La technique d’impression 3D des chercheurs d’Oxford permet de produire des implants sous forme de gouttelettes (mesurant environ 1000 μm de haut et 500 μm de large) imitant un modèle de tissu cortical à 2 couches. Pour ce faire, les hiPSC sont d’abord différenciés en deux sous-types de cellules progénitrices neuronales : l’un spécifique à la couche corticale supérieure et l’autre à la couche profonde. Ces lots de cellules sont ensuite mis en suspension dans une solution afin de former deux sortes de bioencres, permettant d’imprimer le tissu strate par strate. La technique permet de produire des tissus mous structurellement bien définis, composés de cellules et de matrice extracellulaire, le tout sans nécessiter d’échafaudage de soutien.
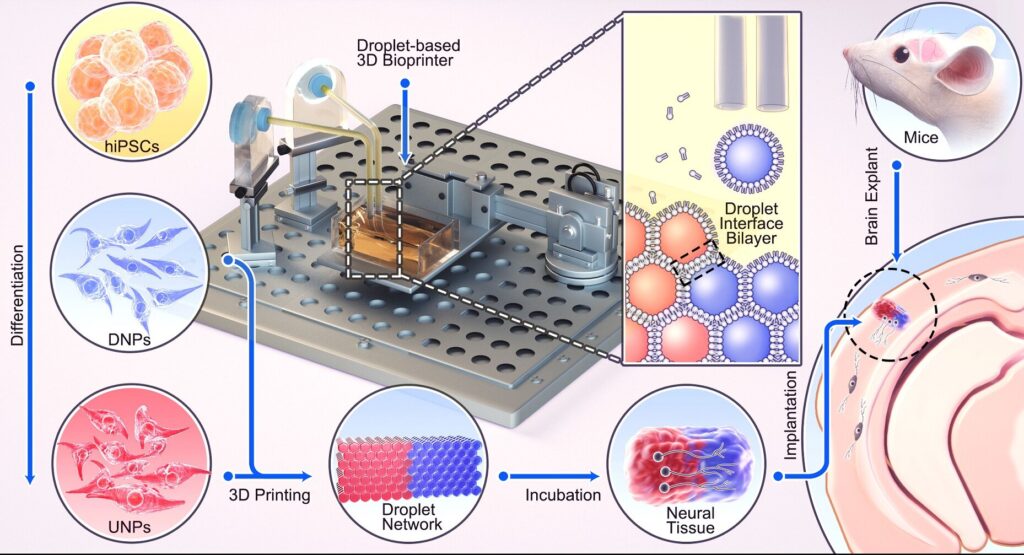
Après impression, les couches de cellules progénitrices peuvent maturer, incluant notamment une différenciation terminale, une croissance et une migration. Les structures résultantes sont ensuite conservées in vitro pendant plusieurs semaines. L’analyse de l’expression de biomarqueurs spécifiques à chaque strate indique que l’architecture superposée est correctement maintenue.
Afin d’évaluer leur capacité à s’intégrer au milieu hôte, les gouttelettes ont été implantées ex vivo dans des cerveaux de souris. Après une semaine, les implants ont bien conservé leur morphologie cellulaire. Les nouvelles cellules ont migré à travers la frontière implant-hôte. L’activité des ions calcium a montré que les implants sont correctement intégrés structurellement et fonctionnellement, au niveau du cerveau des rongeurs. D’après Yongcheng Jin, auteur principal de l’étude et chercheur au département de chimie de l’Université d’Oxford : « cette avancée marque une étape importante vers la fabrication de matériaux présentant la structure et la fonction complètes des tissus cérébraux naturels ».
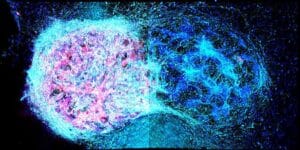


Par ailleurs, l’impression assistée par ordinateur permet de modeler les gouttelettes de sorte à les arranger en réseau multicouches. Par exemple, les chercheurs ont pu superposer un réseau de dimensions 8x8x8 de cellules colorées au RFP (red fluorescent protein) avec autre réseau de dimensions 12x12x12 de cellules marquées par GFP (green fluorescent protein), le tout enveloppé par une couche marquée par RFP. Cette technique a permis de produire des structures tridimensionnelles (cubiques ou d’autres formes) à une échelle inférieure au millimètre. Ainsi, cela pourrait permettre de produire des structures imitant les 6 couches corticales de façon plus précise et naturelle que les implants produits jusqu’ici.
Toutefois, Zoltán Molnár, du département de physiologie, d’anatomie et de génétique de l’Université d’Oxford et coauteur de la nouvelle étude, explique que « le développement du cerveau humain est un processus délicat et élaboré avec une chorégraphie complexe. Il serait naïf de penser que nous pouvons recréer l’intégralité de la progression cellulaire qui y réside ». Néanmoins, la nouvelle technique permet déjà de se rapprocher de la production d’implants personnalisés pouvant résorber efficacement les lésions cérébrales. En outre, elle pourrait fournir des modèles plus élaborés pour les essais médicamenteux in vitro.