Le développement de traitements anticancer est un enjeu de santé publique mondial. En France, le cancer représente la première cause de décès chez l’homme et la deuxième chez la femme. Des scientifiques ont mis au point une nouvelle technique visant à stopper le développement du cancer en tentant de contourner les thérapies anticancéreuses actuelles. En perturbant les composants cellulaires responsables de la conversion de l’oxygène en énergie chimique, les cellules cancéreuses sont éliminées. Une technique innovante et prometteuse.
Le traitement du cancer est un processus à long terme, car les cellules cancéreuses établies dans un organisme évoluent souvent vers des formes agressives et deviennent incurables. Par conséquent, les plans de traitement impliquent souvent plusieurs combinaisons de médicaments et/ou une radiothérapie afin de prévenir la rechute du cancer. Pour lutter contre la variété des types de cellules cancéreuses, de multiples médicaments ont été développés pour cibler des processus biochimiques spécifiques à chaque type de cellule, rendant les thérapies lourdes.
Cependant, les cellules cancéreuses sont très adaptatives et capables de développer des mécanismes pour contourner les effets du traitement. Notamment, elles sont généralement plus actives sur le plan métabolique que les cellules normales, ce qui fait partie de ce qui les aide à devenir incontrôlables et à rendre les traitements mis en place inefficaces. C’est pourquoi les recherches se multiplient, comme la mise au point en 2022 de nanomachines s’attaquant aux cellules cancéreuses, capables de pénétrer au cœur même de ces cellules pour provoquer leur destruction de l’intérieur.
Récemment, des scientifiques de l’Institut Max Planck pour la recherche sur les polymères ont développé une nouvelle méthode de les éliminer en quelques heures seulement. La technique repose sur des molécules autoassemblées asphyxiant littéralement les cellules cancéreuses. Leurs travaux prometteurs sont publiés dans la revue Journal of the American Chemical Society.
Des nanostructures asphyxiantes
Les scientifiques basent leur étude sur l’une des fonctions métaboliques clés des cellules de tous les êtres vivants, appelée la conversion de l’oxygène en ATP (adénosine triphosphate). Cette molécule est le principal vecteur d’énergie dans les cellules, nécessaire aux réactions chimiques du métabolisme, à la locomotion, à la division cellulaire, ou encore au transport actif d’espèces chimiques à travers les membranes biologiques.
Comme mentionné précédemment, la principale contre-mesure aux traitements anticancer est la prolifération des cellules cancéreuses, nécessitant beaucoup d’énergie, c’est pourquoi l’ATP joue un rôle clé. David Ng, de l’Institut Max Planck pour la recherche sur les polymères, explique dans un communiqué : « Nous voulons empêcher une telle adaptation en envahissant le pilier principal de la vie cellulaire — comment les cellules respirent, c’est-à-dire absorbent l’oxygène — et produisent ainsi de l’énergie chimique pour la croissance ». Concrètement, si l’on prive le cancer de cette source d’énergie, on peut le stopper dans son élan métastasique.
Une « drogue » prometteuse
L’équipe de recherche a produit une « drogue » synthétique qui se déplace dans les cellules, où elle réagit aux conditions présentes à l’intérieur et déclenche un processus chimique. Cette drogue est constituée de tripeptides contenant du platine (II). Lorsqu’elle pénètre dans l’environnement cellulaire, elle répond au peroxyde d’hydrogène endogène (produit à l’intérieur de l’organisme) en regroupant ses molécules pour former de minuscules poils, des milliers de fois plus fins qu’un cheveu humain. Les nanostructures formées bloquent les fonctions métaboliques, y compris la glycolyse aérobie et la phosphorylation oxydative, arrêtant ainsi la production d’ATP.
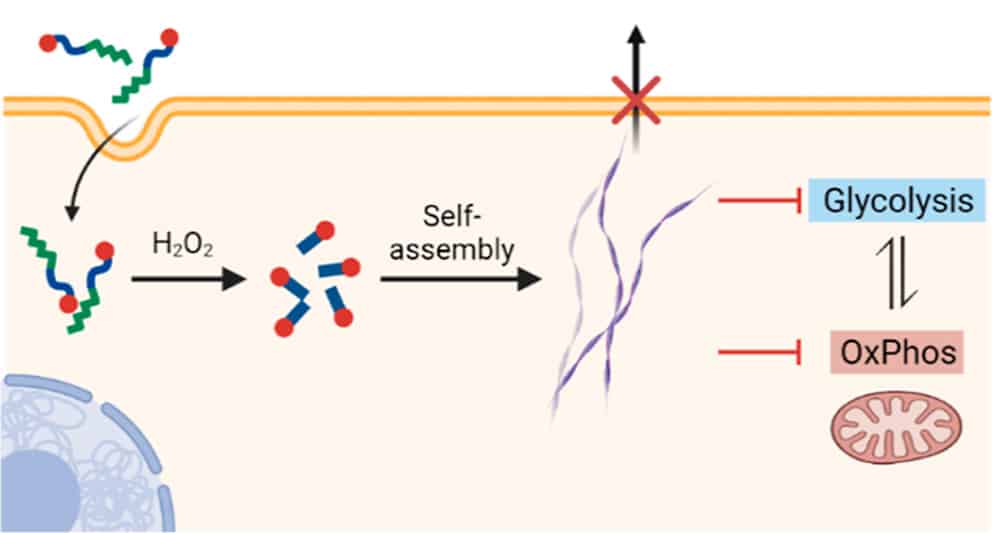
Zhixuan Zhou, de l’Institut Max Planck et premier auteur de l’étude, explique : « Ces poils sont fluorescents, vous pouvez donc les regarder directement au microscope au fur et à mesure de leur formation ».
En effet, les scientifiques ont surveillé la consommation d’oxygène dans différents types de cellules et ont découvert que les poils les empêchaient toutes de convertir l’oxygène en ATP. Le processus a fonctionné même pour les cellules dérivées d’un cancer métastatique incurable.
En conséquence, les cellules meurent rapidement en seulement quatre heures environ. Avec encore quelques années de recherches supplémentaires, les scientifiques espèrent pouvoir développer une nouvelle méthode pour traiter un cancer jusqu’ici incurable.
Weil, Ng et ses collègues, grâce à leurs résultats encourageants dans une culture de laboratoire contrôlée, veulent approfondir leurs connaissances sur la façon dont ces minuscules poils empêchent la conversion de l’oxygène en énergie chimique. Avec un développement ultérieur, ces nanostructures pourraient éventuellement être manipulées pour contrôler d’autres processus cellulaires afin de traiter d’autres maladies graves.
Les auteurs concluent : « En démontrant que les fonctions cellulaires complexes peuvent être traitées uniquement par la formation de nanostructures grâce à des réactions en cascade contrôlées et à l’autoassemblage, nous présentons une nouvelle voie pour relever les grands défis de la découverte de médicaments et de la biologie synthétique ».