En étudiant le comportement de l’eau à très haute pression, une équipe de l’Université du Nevada à Las Vegas (UNLV) a découvert une nouvelle forme de glace, notée Ice-VIIt, dont l’arrangement des atomes n’avait encore jamais été observé. Les chercheurs pensent que cette forme d’eau solide pourrait être particulièrement abondante dans la croûte et le manteau supérieur de certaines exoplanètes, qui de ce fait, pourraient présenter un plus grand potentiel d’habitabilité.
Dans l’eau liquide, bien que les molécules d’eau soient mobiles, chacune s’entoure à chaque instant de quatre autres molécules d’eau (les quatre atomes d’oxygène formant un tétraèdre). Sous 0 °C, à la pression atmosphérique, l’eau liquide passe à l’état solide : cette forme de glace « ordinaire » adopte alors une structure cristalline de type hexagonal, dans laquelle les atomes d’hydrogène sont désordonnés ; cette variété de glace est appelée glace Ih. C’est la glace qui se forme dans nos congélateurs ou qui tombe sous forme de grêle ou de flocons de neige. Sa masse volumique est inférieure à celle de l’eau.
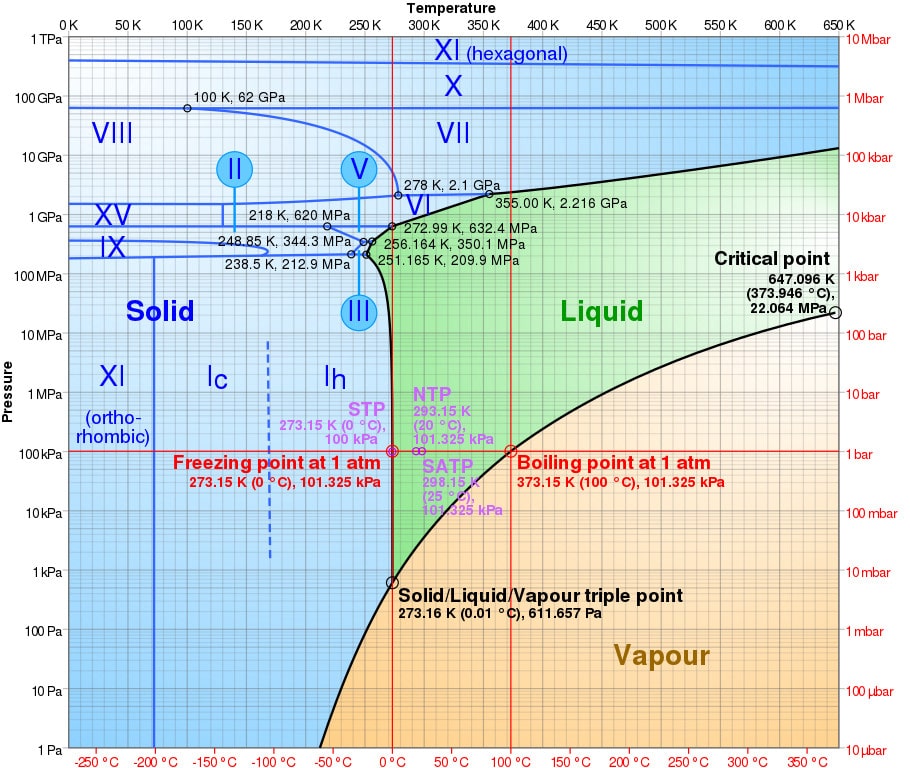
Mais selon les conditions de température et de pression, l’eau peut en réalité former plusieurs autres formes de solides (voir diagramme ci-dessous), plus ou moins stables. Les scientifiques ont déjà identifié plus d’une vingtaine de formes de glace. Sous haute pression en particulier, on recense plus d’une dizaine de formes cristallines (notées ice ou glace II, III, IV, etc.). Contrairement à la glace standard que l’on connaît, ces glaces se caractérisent par une densité supérieure à l’eau liquide correspondante — ce qui signifie que des glaçons faits de cette glace particulière couleraient au fond d’un verre d’eau.
Une transition entre deux phases de glaces connues
Grâce à une nouvelle méthode conçue pour mesurer les propriétés de l’eau à haute pression, les chercheurs du Nevada Extreme Conditions Lab de l’UNLV, ont observé une nouvelle transition de glace d’eau, située entre les phases de glace VII et de glace X déjà bien connues. Pour obtenir cette forme inédite, l’équipe, dirigée par Zachary Grande, a placé un échantillon d’eau dans une cellule à enclumes de diamant — un dispositif qui permet de soumettre un matériau à des pressions et températures extrêmes, l’échantillon pouvant être chauffé par un laser infrarouge jusqu’à 4000 K.
L’échantillon a été compressé entre les deux diamants, jusqu’à ce qu’il se congèle en plusieurs cristaux de glace mélangés. Ils ont ensuite fait fondre temporairement cette glace par laser ; elle s’est alors rapidement resolidifiée sous forme de minuscules cristaux, telle une poudre. Ils ont réitéré l’opération en augmentant peu à peu la pression, faisant fondre la glace périodiquement au laser et observant la manière dont elle se recristallisait — les atomes d’oxygène et d’hydrogène adoptant à chaque fois un arrangement différent.
C’est ainsi qu’ils ont observé la glace passer d’une phase cubique connue (glace VII), à une structure de symétrie tétragonale jamais vue auparavant, notée glace VIIt, avant de se stabiliser dans une autre phase connue (glace X). La transition vers la glace VIIt a été observée à 5,1 ± 0,5 GPa, rapportent les chercheurs dans Physical Review B.
À savoir que la glace VII a été synthétisée pour la première fois en 1937 ; elle a été observée à l’état naturel en 2017, sous la forme d’inclusions dans des diamants extraits d’une mine du Botswana — ces inclusions se sont formées dans le manteau terrestre, à l’état d’eau liquide, qui s’est cristallisée en remontant vers la surface. Il s’agit d’une phase cubique simple, dans laquelle les positions des atomes d’hydrogène sont désordonnées. La glace X, également observée à haute pression, adopte quant à elle une structure cubique centrée.
Une glace qui pourrait être commune sur certaines exoplanètes
Dans la phase de glace VIIt, le réseau cubique de la glace VII est étiré le long de l’un de ses vecteurs de sorte que la structure s’étende en un arrangement rectangulaire, puis elle finit par se stabiliser dans l’arrangement cubique symétrique et entièrement ordonné de la glace X.
Au passage, l’équipe a également découvert que la transition vers la phase X s’est produite à des pressions beaucoup plus faibles (près de trois fois inférieures !) que ce qui était attendu : la transition de symétrisation des liaisons hydrogène s’est produite à une pression de 30,9 ± 3 GPa, précisent-ils.
Or, cette transition particulière est sujette à débat depuis plusieurs décennies parmi les physiciens — de précédents travaux de recherche situaient cette pression de transition entre 40 et 120 GPa. « Les travaux de Zach ont démontré que cette transformation vers un état ionique se produit à des pressions beaucoup, beaucoup plus faibles que ce que l’on pensait auparavant. C’est la pièce manquante, et les mesures les plus précises jamais réalisées sur l’eau dans ces conditions », souligne Ashkan Salamat, physicien de l’UNLV.
Étant donné les conditions nécessaires à sa formation, on ne peut observer la glace VIIt à la surface de la Terre. En revanche, les chercheurs estiment qu’elle pourrait être relativement commune dans le manteau terrestre, ainsi que dans les grandes lunes et les planètes riches en eau en dehors de notre système solaire. Cette découverte remet ainsi en question le potentiel d’habitabilité de certaines exoplanètes.


