En mars 2017, selon l’OMS, environ 300 millions de personnes souffraient de dépression dans le monde, en faisant la maladie psychique la plus répandue. Se présentant avec une gamme de symptômes divers et une sévérité variable, la dépression est un trouble qui ne doit pas être sous-estimé. Même si de nombreuses molécules antidépressives existent actuellement, beaucoup sont inefficaces dans certaines formes graves ou résistantes. Récemment, une équipe de chercheurs israéliens a montré que cibler les canaux potassiques cérébraux KCNQ2/3 constituait une nouvelle voie thérapeutique permettant de lutter contre la dépression et ses symptômes.
Des chercheurs de l’école de médecine Icahn du mont Sinaï ont identifié un médicament qui agit contre la dépression par un mécanisme complètement différent des traitements existants. Leur étude a montré que l’ézogabine (également connue sous le nom de retigabine), un médicament qui ouvre les canaux potassiques de type KCNQ2/3 dans le cerveau, est associée à des améliorations significatives des symptômes dépressifs et de l’anhédonie chez les patients souffrant de dépression.
L’anhédonie est la capacité réduite à éprouver du plaisir ou le manque de réactivité à des stimuli agréables ; il s’agit d’un symptôme central de la dépression et associé à des formes sévères, à une mauvaise réponse aux antidépresseurs et à un risque accru de suicide. L’ézogabine a été approuvée par la Food and Drug Administration des États-Unis en 2011 comme anticonvulsivant pour le traitement de l’épilepsie, mais n’avait pas été étudiée auparavant dans la dépression.
Les résultats de la recherche, publiés dans la revue American Journal of Psychiatry, fournissent des preuves initiales chez l’humain du canal KCNQ2/3 en tant que nouvelle cible pour la découverte de nouvelles molécules pour la dépression et l’anhédonie.
« Notre étude est le premier essai randomisé contrôlé par placebo à montrer qu’un médicament affectant ce type de canal ionique dans le cerveau peut améliorer la dépression et l’anhédonie chez les patients. Le ciblage de ce canal représente un mécanisme d’action complètement différent de tout autre traitement antidépresseur actuellement disponible », déclare James Murrough, professeur de psychiatrie et de neurosciences, directeur du centre de découverte et de traitement de la dépression et de l’anxiété à l’Icahn School of Medicine.
Canaux KCNQ2/3 : ils sont directement impliqués dans le mécanisme dépressif
La nouvelle cible médicamenteuse, le canal KCNQ2/3, fait partie d’une grande famille de canaux ioniques appelés « famille KCNQ » (ou Kv7) qui agissent en tant que contrôleurs importants de l’excitabilité et du fonctionnement des cellules cérébrales dans le système nerveux central. Ces canaux affectent le fonctionnement des cellules cérébrales en contrôlant le flux de la charge électrique à travers la membrane cellulaire sous forme d’ions potassium (K+).
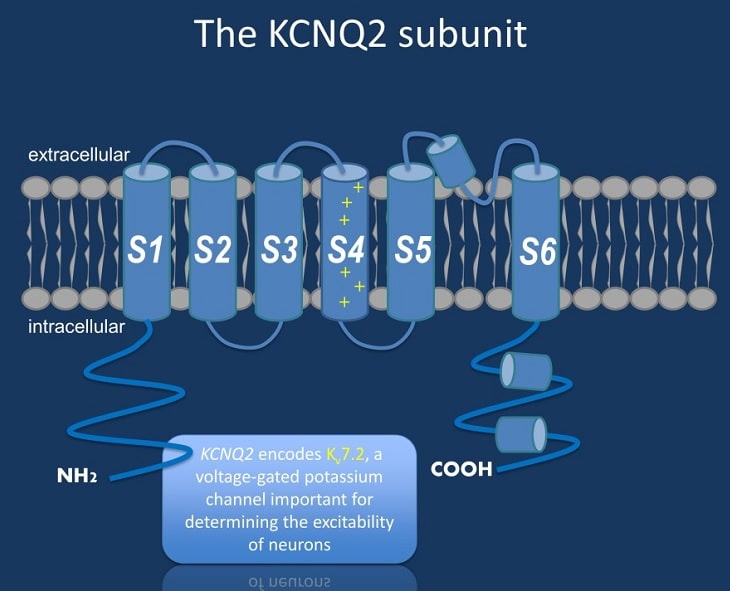
Des chercheurs du mont Sinaï avaient précédemment mené une série d’études chez la souris montrant que les changements dans le canal potassique KCNQ2/3 jouent un rôle important dans la tendance des animaux à montrer une dépression et un comportement anhédonique suite à un stress chronique dans un modèle expérimental de dépression. En particulier, les souris qui semblent résistantes au développement de la dépression face au stress montrent une augmentation des canaux KCNQ2/3 dans le cerveau.
« Nous avons considéré le fonctionnement amélioré du canal KCNQ comme un mécanisme moléculaire potentiel de résilience au stress et à la dépression », indique Ming-Hu Han, professeur de neurosciences, qui a également découvert que s’il donnait un médicament qui pourrait augmenter l’activité de ce canal, comme l’ézogabine, à des souris devenues déprimées dans le modèle de stress, les souris ne présentaient plus de dépression et de comportements anhédoniques ; en d’autres termes, le médicament a agi comme un antidépresseur.
L’effet bénéfique de l’ézogabine sur les symptômes de la dépression
L’étude actuelle était un essai clinique de preuve de concept en deux sites, en double aveugle, randomisé et contrôlé par placebo, conçu comme un test préliminaire de l’hypothèse selon laquelle l’augmentation de l’activité des canaux KCNQ2/3 dans le cerveau est une nouvelle approche viable pour le traitement de la dépression. Quarante-cinq patients adultes diagnostiqués avec un trouble dépressif ont été affectés à une période de traitement de cinq semaines avec une dose quotidienne d’ézogabine ou un placebo correspondant.
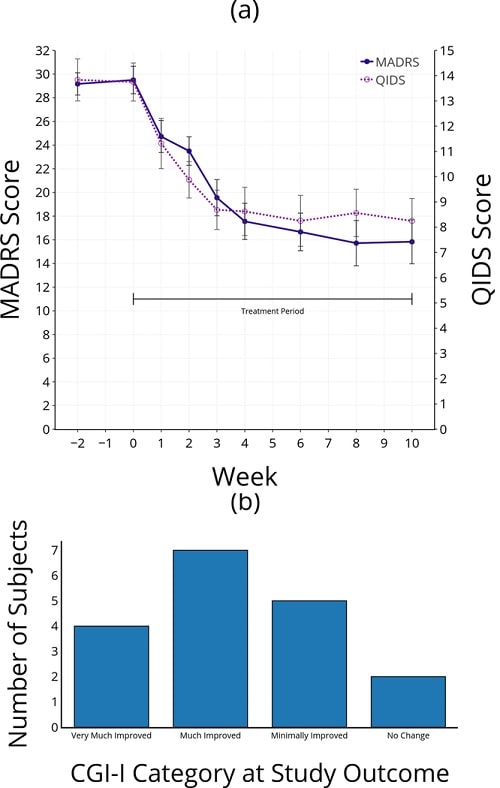
Tous les participants ont subi des évaluations cliniques et une imagerie par résonance magnétique fonctionnelle (IRMf) au cours d’une tâche de récompense au départ et à la fin de la période de traitement. Par rapport aux patients traités par placebo, ceux traités par ézogabine ont montré une réduction significative et importante de plusieurs mesures clés de la gravité de la dépression, de l’anhédonie et de la gravité globale de la maladie.
Par exemple, des améliorations significatives après le traitement par ézogabine par rapport au placebo ont été observées à l’aide de l’échelle d’évaluation de la dépression de Montgomery-Asberg (MADRS), du Quick Inventory of Depressive Symptomatology-Self Report (QIDS-SR), de la Snaith-Hamilton Pleasure Scale (SHAPS) et de la Temporal Experience of Pleasure Scale (TEPS). Le groupe ézogabine a également montré une tendance à une augmentation de la réponse à l’anticipation de la récompense dans le cerveau par rapport au placebo, bien que cet effet n’ait pas atteint une signification statistique.
Vers le développement de traitements plus efficaces
En collaboration avec Han, Murrough a mené une série d’études chez des patients souffrant de dépression pour commencer à tester si les observations chez la souris pouvaient être traduites chez l’humain. Une première étude ouverte (sans placebo) chez des patients souffrant de dépression, dirigée par Murrough, a fourni des preuves initiales que l’ézogabine pouvait améliorer les symptômes de la dépression et de l’anhédonie d’une manière qui était associée à des changements dans la fonction cérébrale.
« Je pense qu’il est juste de dire que la plupart d’entre nous, membres de l’équipe d’étude, avons été assez surpris par l’importance de l’effet bénéfique de l’ezogabine sur les symptômes cliniques à travers de multiples mesures liées à la dépression. Nous sommes très encouragés par ces résultats et l’espoir qu’ils offrent dans la perspective de développer de nouveaux traitements efficaces contre la dépression et les troubles associés. De nouveaux traitements sont nécessaires de toute urgence étant donné que plus d’un tiers des personnes souffrant de dépression ne sont pas correctement traitées avec les thérapies actuellement approuvées », conclut Murrough.


