Des chercheurs développent un nouveau traitement, basé sur l’utilisation de peptides, visant à duper le coronavirus avant qu’il n’infecte les cellules. L’idée est de produire des structures similaires aux récepteurs ACE2 (que le SARS-CoV-2 utilise pour infecter les cellules, en s’y accrochant avec sa protéine Spike) afin de capturer le virus avant qu’il ne s’accroche aux véritables cellules. Ainsi, il s’agit d’éliminer la menace avant même qu’elle ait pu envahir l’hôte.
Pour cela, ils ont mis au point des fragments de protéines (des peptides) qui s’insèrent parfaitement dans une rainure de la protéine Spike du SARS-CoV-2, qu’elle utiliserait normalement pour accéder à une cellule hôte. En effet, les recherches antérieures ont permis de déterminer que le nouveau coronavirus se lie à une protéine réceptrice à la surface des cellules ciblées, appelée ACE2. Ce récepteur est situé sur certains types de cellules humaines dans les poumons et les fosses nasales, fournissant au coronavirus de nombreux points d’accès pour infecter l’organisme.
Des chercheurs de l’université d’État de l’Ohio ont donc conçu et testé des peptides, appelés Spike-targeting ACE2-derived peptides (SAPs), qui ressemblent suffisamment à l’ACE2 pour convaincre le coronavirus de s’y lier, une action qui bloque la capacité du virus à pénétrer réellement à l’intérieur de la cellule. « Notre objectif est que chaque fois que le SARS-CoV-2 entre en contact avec les peptides, le virus soit inactivé », a déclaré Amit Sharma, co-auteur de l’étude et professeur adjoint de biosciences vétérinaires pour l’État de l’Ohio. « Pour ce faire, nous devons atteindre le virus alors qu’il est encore en dehors de la cellule ».
L’équipe de l’État de l’Ohio envisage d’administrer ces peptides manufacturés sous forme de spray nasal ou d’aérosol désinfectant de surface, entre autres applications, pour bloquer les points d’accès du SARS-CoV-2 en circulation avec un agent qui empêche leur entrée dans les cellules cibles. « Avec les résultats que nous avons obtenus avec ces peptides, nous sommes sur la bonne voie pour passer aux étapes de développement du produit », déclare Ross Larue, co-auteur principal et professeur assistant de recherche en pharmacie et pharmacologie dans l’État de l’Ohio.
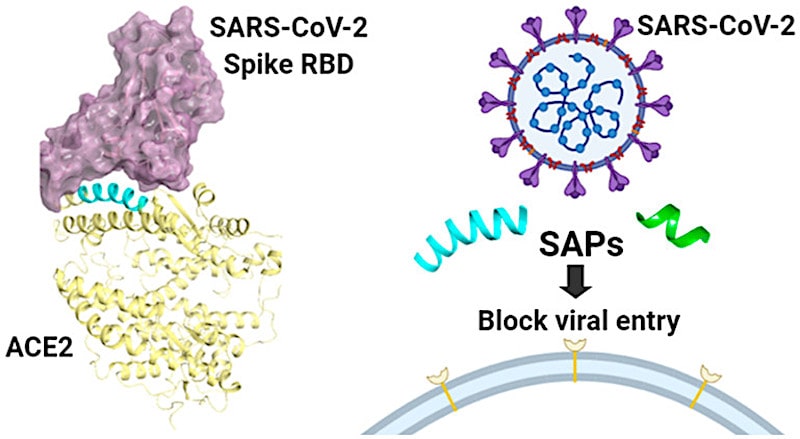
Le SARS-CoV-2, comme tous les autres virus, a besoin d’accéder à des cellules vivantes. Pour cela, les virus détournent les fonctions des cellules pour faire des copies d’eux-mêmes et provoquer l’infection. Une réplication virale très rapide peut submerger le système hôte avant que les cellules immunitaires ne puissent se défendre efficacement.
L’une des raisons pour lesquelles ce coronavirus est si infectieux est qu’il se lie très étroitement au récepteur ACE2, qui est abondant sur les cellules humaines et de certaines autres espèces. La protéine Spike à la surface du SARS-CoV-2, qui est devenue sa caractéristique la plus reconnaissable, est également fondamentale pour son succès à se fixer à l’ACE2. Les progrès récents en matière de cristallisation des protéines et de microscopie ont permis de créer des images informatiques de structures protéiques spécifiques, seules ou en combinaison, comme lorsqu’elles se lient les unes aux autres.
Une conception minutieuse et des résultats prometteurs
Sharma et ses collègues ont examiné de près les images de la protéine de pointe du SARS-CoV-2 et de l’ACE2, en étudiant précisément la façon dont leurs interactions se produisent et les connexions nécessaires pour que les deux protéines se fixent. Ils ont remarqué qu’une queue en forme de ruban spiralé sur l’ACE2 était le point clé de l’attachement, qui est devenu le point de départ de la conception des peptides.
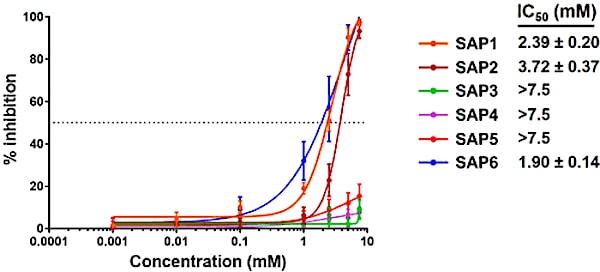
« La plupart des peptides que nous avons conçus sont basés sur le ruban en contact avec la protéine Spike », a déclaré Sharma, qui est également professeur dans le domaine des infections microbiennes et de l’immunité. « Nous nous sommes concentrés sur le développement de peptides les plus courts possibles avec le minimum de contacts essentiels ».
L’équipe a testé plusieurs peptides comme « inhibiteurs compétitifs » qui pourraient non seulement se lier de manière sûre aux protéines Spike du SARS-CoV-2, mais aussi empêcher ou réduire la réplication virale dans les cultures cellulaires. Deux peptides, l’un avec les points de contact minimaux et l’autre plus grand, ont été efficaces pour réduire l’infection par le SARS-CoV-2 dans les études cellulaires par rapport aux témoins.
Sharma a décrit ces résultats comme le début d’un processus de développement de produit, qui sera poursuivi par l’équipe de virologues et de chimistes pharmaceutiques qui collaborent sur ce projet. « Nous adoptons une approche sur plusieurs fronts », précise Sharma. « Avec ces peptides, nous avons identifié les contacts minimaux nécessaires pour inactiver le virus. À l’avenir, nous prévoyons de nous concentrer sur le développement de certains aspects de cette technologie à des fins thérapeutiques ».
« L’objectif est de neutraliser le virus efficacement et puissamment, et maintenant, en raison de l’émergence de variantes, nous sommes intéressés par l’évaluation de notre technologie par rapport aux mutations émergentes », conclut Sharma.