Depuis plusieurs années, les méthodes d’édition génétique se développent considérablement, CRISPR-Cas9 tenant le haut du podium. Si cette technique permet d’éditer et modifier certains éléments du génome, une nouvelle version de celle-ci, CRISPR-Cas3, permet quant à elle de cibler et détruire certains segments d’ADN spécifiques. Cela pourrait permettre de neutraliser des virus et soigner des infections virales comme l’herpès ou l’hépatite B.
La nouvelle technique s’appelle CRISPR-Cas3, et les chercheurs de l’université Cornell pensent qu’elle pourrait être utilisée pour traiter les maladies virales. Les scientifiques ont utilisé Cas3 pour identifier et détruire de longs segments d’ADN humain, selon une étude publiée dans la revue Molecular Cell.
Au lieu de localiser et d’extraire du matériel génétique de la même manière que CRISPR-Cas9, la nouvelle méthode localise les séquences d’ADN et supprime en réalité des segments entiers. Ce système peut potentiellement rechercher et éliminer des virus ectopiques tels que l’herpès simplex, Epstein-Barr et l’hépatite B, qui constituent chacun une menace majeure pour la santé publique.
La technologie CRISPR-Cas3 permet également aux chercheurs d’analyser le génome et de détecter des éléments génétiques non codants, qui constituent 98% de notre génome mais n’ont pas été bien caractérisés. Ces éléments agissent comme des régulateurs qui contrôlent l’expression des protéines dans les gènes codants. Ils se sont révélés être essentiels pour la différenciation cellulaire et la détermination du sexe.
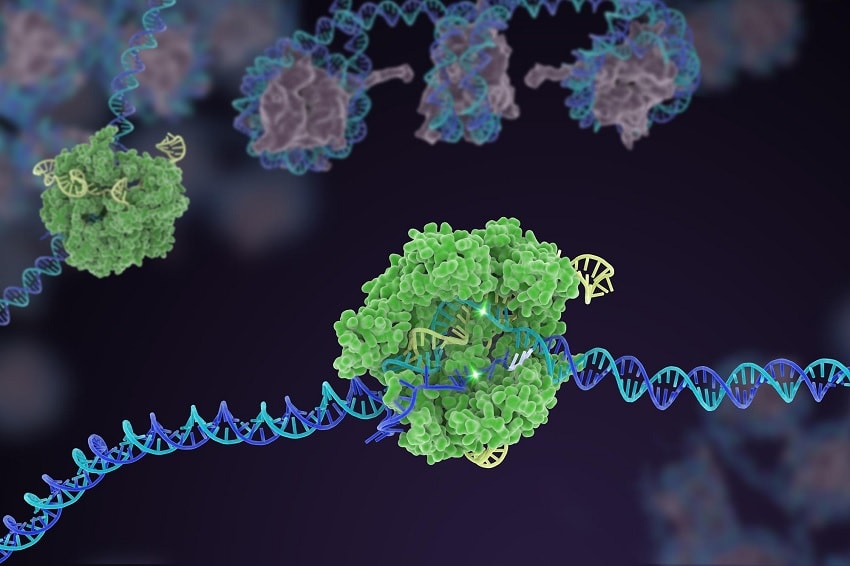
CRISPR-Cas3 pourrait être utilisé pour cribler efficacement des éléments génétiques non codants et pour effacer de longues séquences d’ADN. Une fois effacés, les scientifiques peuvent rechercher les fonctions manquantes dans un organisme afin de déterminer le rôle de cet élément génétique.
Sur le même sujet : Cette vidéo montre CRISPR éditer de l’ADN en temps réel
« Mon laboratoire a passé 10 ans à comprendre le fonctionnement de CRISPR-Cas3. Je suis ravi que mes collègues et moi ayons enfin démontré son activité de modification du génome dans les cellules humaines » déclare le biologiste moléculaire Cornell Ailong Ke. « Nos outils peuvent être conçus pour cibler des virus de manière très spécifique, puis pour les effacer de manière très efficace. En théorie, cela pourrait permettre de guérir des maladies virales ».
Les systèmes CRISPR-Cas9 utilisent un ARN bactérien comme guide, qui reconnaît et s’apparie à une séquence d’ADN. Lorsqu’une correspondance est trouvée, l’ARN guide dirige les protéines associées à CRISPR (Cas) vers cette chaîne précise d’ADN. Une fois localisée, la protéine Cas9 coupe l’ADN cible au bon endroit. CRISPR-Cas3 utilise le même mécanisme pour localiser une séquence spécifique d’ADN. Cependant, au lieu de couper l’ADN en deux, sa nucléase efface l’ADN en continu, jusqu’à 100 kilobases.
Pour la première fois, Ke, Zhang et ses collègues ont supprimé avec succès des séquences de 100 kilobases d’ADN ciblées dans des cellules souches embryonnaires humaines et dans un autre type de cellule appelé HAP1.
Bien que CRISPR-Cas3 recèle le potentiel d’un outil d’édition du génome plus puissant que CRISPR-Cas9, les chercheurs s’efforcent de contrôler la longueur de suppression d’une section. « Nous ne pouvons pas définir avec précision les limites de suppression, et c’est un problème en matière de traitement » conclut Ke.