Au nombre des maladies auto-immunes, le diabète de type 1 est l’une des pathologies les plus répandues. Depuis de nombreuses années, les scientifiques savent que cette maladie a pour origine une réponse immunitaire anormale de l’organisme, qui attaque ses propres cellules. Cependant, les mécanismes sous-jacents demeuraient encore flous. Récemment, la découverte d’un lymphocyte hybride par des chercheurs américains pourrait enfin expliquer, du moins en partie, ce mécanisme d’auto-immunité.
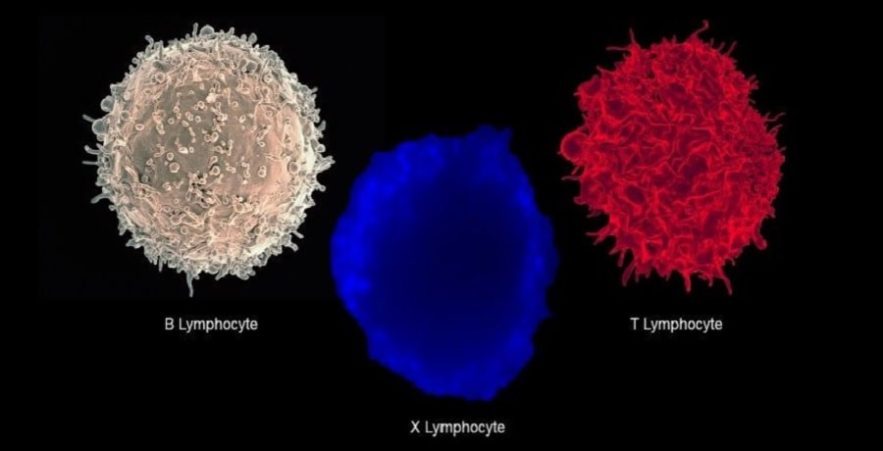
Des recherches menées par une équipe de la faculté de médecine de l’Université Johns Hopkins ont permis d’identifier une variété unique de globules blancs présentant les caractéristiques de deux des cellules les plus importantes de notre système immunitaire. « La cellule que nous avons identifiée est un hybride entre les deux principaux moteurs du système immunitaire adaptatif, les lymphocytes B et les lymphocytes T » explique le pathologiste Abdel-Rahim A. Hamad, de la faculté de médecine de l’Université Johns Hopkins.
Ensemble, ces deux types de lymphocytes chassent les envahisseurs et les cellules anormales menaçant notre organisme. Les cellules B jouent le rôle de répartiteur en fournissant des détails importants qui aident à identifier ces menaces. Après avoir mûri dans la moelle osseuse, ils se rendent dans des endroits tels que les ganglions lymphatiques, où ils se familiarisent avec des signatures chimiques appelées antigènes — des fragments laissés par des menaces passées.
Les lymphocytes B et T : acteurs principaux de la réponse auto-immunitaire
En utilisant ces caractéristiques d’identification, ils produisent des anticorps qui peuvent alerter le corps dans le cas où la même menace se présenterait à nouveau par la suite. Les lymphocytes T, quant à eux, suivent les directives des lymphocytes B et, une fois la menace identifiée par ces derniers, sont chargés de la détruire. La variété connue sous le nom de cellule T cytotoxique ou « tueuse », recherche dans le corps des cellules contenant des antigènes à leur surface et les détruit avant qu’elles ne puissent nuire.
Un autre type de cellule T appelé « assistant » demande aux cellules B immatures de se préparer « à la guerre » en se divisant rapidement et en se dirigeant vers le terrain où elles peuvent distribuer des anticorps. Ces actions dépendent d’un ensemble complexe d’hormones et d’interactions impliquant des récepteurs cellulaires spécifiques — et parfois des erreurs se produisent.
Sur le même sujet : Des cellules souches pour lutter contre le diabète
Un exemple est lorsque les cellules T répondent à l’insuline comme s’il s’agissait d’un antigène. Les chercheurs ont émis l’hypothèse que c’était la principale cause du diabète de type 1, dans lequel les cellules des îlots producteurs d’insuline dans le pancréas étaient détruites par une attaque immunitaire.
Cela implique un type de cellule présentatrice d’antigène, qui comprend les macrophages et les cellules B, avec un marqueur de surface variant communément associé à des affections auto-immunes telles que le diabète et la maladie cœliaque, appelées DQ8. L’insuline se lie à DQ8, ce qui, hypothétiquement, provoquerait le recrutement de lymphocyte T tueurs dirigés contre ce complexe. « Cependant, nos expériences indiquent qu’il s’agit d’une liaison faible et non susceptible de déclencher une forte réaction immunitaire conduisant au diabète de type 1 » déclare Hamad.
Un lymphocyte hybride potentiellement à l’origine du diabète de type 1
À l’aide d’échantillons de sang prélevés sur des volontaires recrutés par l’intermédiaire du Johns Hopkins Comprehensive Diabetes Center, les chercheurs sont tombés sur une étrange population de globules blancs affichant les récepteurs des cellules T et B. Une analyse plus poussée a révélé que ces cellules avaient des gènes exprimés de manière unique, ainsi que l’activation des types de gènes associés à chaque lignée cellulaire. Et notamment un lymphocyte combinant les deux propriétés B et T.
« Cela accentue probablement la réponse auto-immune car un seul lymphocyte remplit simultanément les fonctions qui nécessitent normalement l’action concertée de deux » explique Hamad. L’équipe a découvert les récepteurs des cellules B sur cette étrange cellule à double expression (DE) codée pour une protéine qui pourrait aider à expliquer l’hyper-réaction d’insuline. Les résultats ont été publiés dans la revue Cell.
Sur la base de simulations informatiques, la protéine — appelée x-Id — se lie à DQ8 avec une force mille fois supérieure à celle de l’insuline. Il en résulte une augmentation considérable de la réponse des cellules T, ce qui pourrait potentiellement conduire leur guerre contre les cellules pancréatiques.
Une nouvelle voie pour mieux comprendre le mécanismes des maladies auto-immunes
« Cette découverte, combinée à notre conclusion selon laquelle le peptide x-Id amorce les cellules T à diriger l’attaque sur les cellules productrices d’insuline, soutient fortement une connexion entre les cellules DE et le diabète de type 1 » indique Hamad. Les globules blancs peptidiques et hybrides étaient plus susceptibles de se retrouver dans le sang des patients diabétiques, ce qui accroissait la probabilité qu’ils puissent être responsables de la maladie à un certain niveau.
Ce n’est pas seulement le diabète de type 1 qui pourrait enfin être mieux compris. Les chercheurs ont émis l’hypothèse que ces cellules DE pourraient jouer un rôle dans d’autres maladies auto-immunes telles que la sclérose en plaques et la polyarthrite rhumatoïde. Des recherches supplémentaires aideront à confirmer les actions de la cellule et pourraient même donner un aperçu des traitements précoces potentiels pour ces affections immunitaires.