Deux médicaments initialement destinés au cancer et approuvés par la Food and Drug Administration américaine (FDA) ont régénéré les cellules bêta-pancréatiques endommagées par le diabète de type 1 en seulement 48 heures lors d’expériences in vitro. Les nouvelles cellules, générées sur la base de tissus de patients diabétiques, ont correctement sécrété de l’insuline en réponse à l’exposition au glucose. Cette voie de régénération serait viable pour une tranche d’âge allant de 7 à 61 ans au moins (les limites d’âge de l’étude), et pourrait à terme réduire la dépendance aux injections quotidiennes d’insuline.
On estime que plus de 530 millions de personnes souffrent de diabète (toutes causes confondues) dans le monde — un nombre qui devrait passer à 643 millions d’ici 2030. En cas de diabète de type 2 (DT2), l’organisme devient résistant aux effets de l’insuline tout en perdant progressivement sa capacité à en produire. Cette forme de diabète combine ainsi une perte d’efficacité et une insuffisance de production de l’hormone.
En revanche, en cas de diabète de type 1 (DT1, ou diabète insulinodépendant), les cellules bêta-pancréatiques responsables de la synthèse, de la libération et du stockage de l’insuline subissent une destruction irréversible et d’origine auto-immune. Cette condition implique que les patients doivent quotidiennement surveiller leur glycémie et s’administrer de l’insuline afin de la réguler. Bien que cette technique permet de contrôler la glycémie, elle ne permet pas d’inverser ni de ralentir la perte de cellules bêta.
Les traitements actuels pour lutter activement contre la maladie se concentrent sur la régénération des cellules bêta, incluant par exemple des techniques telles que la transplantation d’amas (ou îlots) de ces cellules. Cependant, bien que ces stratégies aient démontré une certaine efficacité, elles se heurtent à d’importants défis liés à la pénurie de donneurs et aux effets secondaires inhérents aux transplantations (dus aux médicaments immunosuppresseurs). D’un autre côté, les résultats positifs obtenus semblent relativement hasardeux, sans compter que les mécanismes épigénétiques régissant cette voie régénérative sont encore mal compris. Cela a conduit à l’exploration d’autres stratégies pouvant stimuler cette régénération.
Des traitements initialement approuvés pour le cancer
Parmi les différentes stratégies explorées figure la restauration de l’expression du gène de l’insuline. Cela serait en théorie possible en intervenant à partir des cellules canalaires pancréatiques, en inhibant l’amplificateur de zeste homologue 2 (EZH2) à l’aide de molécules pharmacologiques actuellement disponibles. L’EZH2 est la sous-unité catalytique du complexe répressif polycomb 2 (une enzyme), régulant l’expression génétique des cellules. Elle est essentielle à la régénération, à la maintenance et à la différenciation de ces dernières en lignées spécifiques.
Sa surexpression entraîne la suppression des gènes responsables du contrôle du cycle cellulaire, entraînant une croissance incontrôlée dans certaines formes de cancer. L’utilisation de ces types traitement pour le DT1 permettrait de stimuler les cellules progénitrices canalaires (les cellules exocrines tapissant la paroi des canaux délivrant les enzymes pancréatiques), de sorte qu’elles se différencient en nouvelles cellules bêta.
Des traitements exploitant cette voie, tels que le GSK126 et le tazemetostat, sont approuvés par la FDA pour le traitement du cancer. La nouvelle étude, codirigée par l’Université Monash et le Baker Heart and Diabetes Institute de Melbourne (Australie), corrobore l’hypothèse selon laquelle cette stratégie pourrait être efficace pour traiter le DT1 et explore les effets de ces deux traitements sur les cellules pancréatiques.
Une régénération possible des cellules entre 7 et 61 ans au moins
Dans le cadre de leur étude, détaillée dans la revue Signal Transduction and Targeted Therapy, les chercheurs australiens ont évalué la capacité du GSK126 et du tazemetostat à réactiver les cellules progénitrices canalaires. Pour ce faire, des échantillons provenant de 3 donneurs âgés de 7, de 56 et de 61 ans ont été prélevés. Le premier souffrait de DT1 depuis le mois précédant l’étude, tandis que le dernier en souffrait depuis 33 ans. Le second était un témoin sain.
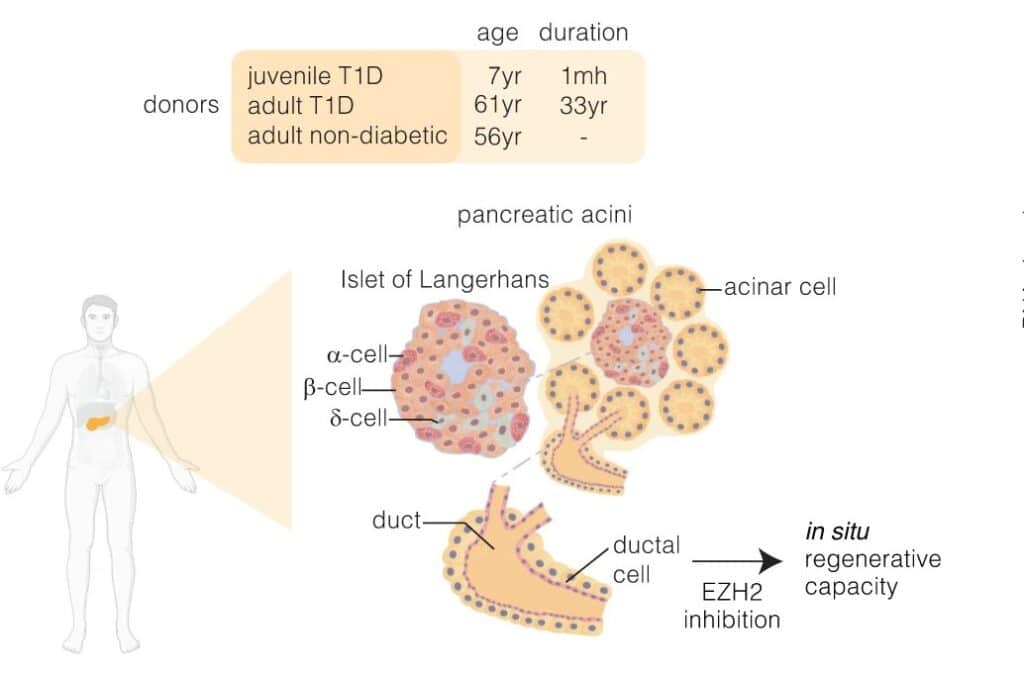
Les chercheurs ont constaté que les cellules progénitrices jeunes et matures se différenciaient correctement en cellules bêta, après exposition aux traitements. En d’autres termes, la régénération des cellules bêta est réalisable entre 7 et 61 ans au moins, ce qui constitue un précieux indice concernant les mécanismes sous-jacents à cette restauration.
Malgré la perte des cellules bêta induite par la maladie, la stimulation des cellules canalaires a restauré l’expression du gène amorçant la production d’insuline. Après seulement 48 heures de stimulation, les nouvelles cellules bêta obtenues ont produit l’hormone avec succès après une exposition au glucose. La prochaine étape de l’étude consistera à reproduire ces résultats sur des modèles précliniques. En outre, l’approbation des traitements par la FDA pourrait faciliter et accélérer leur application clinique.