Le glioblastome est la tumeur primaire cérébrale maligne la plus agressive et la plus fréquente chez l’adulte. L’espérance de vie n’est que de 15 à 17 mois après le diagnostic, et le taux de survie à cinq ans de 5%. En effet, ce cancer réapparait presque toujours après le traitement. La raison principale est l’impossibilité pour les chirurgiens de retirer toutes les cellules souches tumorales, qui peuvent alors persister dans le cerveau. L’enjeu des recherches actuelles est donc d’y remédier. Récemment, des scientifiques américains ont créé un nouvel hydrogel injectable pour prévenir la rechute du glioblastome après une intervention chirurgicale, en entraînant le système immunitaire à traquer ces cellules cancéreuses résiduelles. Cette découverte établit une stratégie thérapeutique locale, pleine d’espoir.
Le glioblastome est un cancer qui se développe dans le cerveau ou la moelle épinière. C’est la forme la plus agressive de l’astrocytome, type de gliome qui prend naissance dans les cellules gliales appelées « astrocytes ». Celles-ci ont un rôle de soutien et de protection des neurones, les cellules nerveuses du cerveau.
Chaque année, on estime qu’environ 2400 nouveaux cas de glioblastome sont diagnostiqués en France. Touchant majoritairement l’adulte, il est plus fréquent chez l’homme que chez la femme. 70% des cas concernent des personnes de 45 à 70 ans et l’âge moyen au diagnostic est de 58 ans. Son traitement n’améliore que très peu les chances de survie des patients. En effet, ce cancer revient presque toujours — généralement quelques mois après l’ablation chirurgicale de la tumeur cérébrale initiale d’un patient. C’est pourquoi les taux de survie pour ce cancer ne sont que de 25% à un an et chutent à 5% au bout de cinq ans.
Comme l’explique dans un communiqué Quanyin Hu, professeur adjoint à la division des sciences pharmaceutiques de la faculté de pharmacie de l’Université du Wisconsin-Madison, et auteur principal de la présente étude : « Une caractéristique du glioblastome est que les cellules tumorales sont très agressives et qu’elles vont infiltrer les tissus environnants. Ainsi, le chirurgien ne peut pas clairement sentir les limites entre la tumeur et le tissu normal, et vous ne pouvez pas en retirer autant que possible, car tous les tissus du cerveau sont extrêmement importants – vous ne voulez certainement pas en retirer trop. Ainsi, la tumeur reviendra, et cela diminue fortement le taux de survie après le traitement ».
Récemment, Quanyin Hu et ses collègues ont mis au point un hydrogel stimulant le système immunitaire des patients. Il peut être injecté dans le cerveau après une intervention chirurgicale pour éliminer les cellules souches cancéreuses restantes. Leurs résultats sont publiés dans la revue Science Translational Medicine.
Un hydrogel booster d’immunité
De manière concrète, l’équipe a créé un hydrogel injectable dans la cavité cérébrale laissée par la tumeur excisée. La méthode d’administration de l’hydrogel fonctionne bien, car elle remplit complètement la cavité cérébrale, puis libère lentement le médicament dans les tissus environnants et favorise la réponse immunitaire anticancéreuse.
C’est pourquoi l’hydrogel est rempli de nanoparticules conçues pour entrer dans et reprogrammer certains types de cellules immunitaires appelées macrophages. Ces cellules immunitaires éliminent normalement les agents infectieux dans le corps. Mais dans l’environnement tumoral, elles peuvent se transformer en une forme qui supprime le système immunitaire et favorise la croissance du cancer. Et à cause de l’inflammation laissée par la chirurgie, ces macrophages, déviant de leur but premier, affluent vers le site chirurgical, alimentant potentiellement une rechute du cancer.
Hu déclare : « Nous voulons tirer parti de ces macrophages et les transformer d’ennemis en alliés ». En modifiant l’environnement tumoral, on induit un changement au niveau des macrophages, de sorte qu’ils ne contribuent plus à favoriser la croissance du cancer, mais recherchent et ciblent les cellules résiduelles, laissées par la chirurgie, et les éliminent. Ils stimulent ainsi une réponse immunitaire antitumorale adaptative, localement et à long terme.
La stratégie « CAR » à la base de l’hydrogel, espoir pour d’autres cancers
Pour atteindre leur but, les chercheurs ont inclus dans l’hydrogel des nanoparticules porteuses de gènes CAR (récepteur d’antigène chimérique — créé artificiellement), spécifiques aux cellules cancéreuses résiduelles. Ces nanoparticules peuvent modifier les macrophages afin qu’ils ciblent une glycoprotéine appelée CD133, un marqueur des cellules souches cancéreuses. L’équipe de Hu a également ajouté un anticorps, CD47, qui bloque un signal des cellules cancéreuses, pour inciter les macrophages à les reconnaître en tant qu’élément à éliminer.
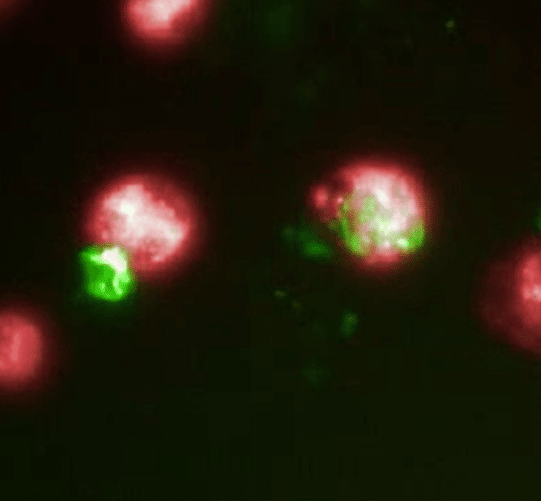
Ainsi, les résultats précliniques dans des modèles de souris montrent que le traitement à l’hydrogel a généré avec succès des macrophages CAR spécifiques aux cellules souches du gliome — en créant essentiellement les cellules immunitaires sur place pour cibler et tuer toutes les cellules souches de gliome persistantes.
La prochaine étape de Hu consiste à tester l’hydrogel dans des modèles animaux plus grands et à surveiller également l’efficacité et la toxicité à long terme au-delà de la période initiale de quatre à six mois.
Hu souligne : « Nous avons beaucoup de travail à faire avant que cela puisse être potentiellement traduit en clinique, mais nous sommes convaincus qu’il s’agit d’une approche très prometteuse pour apporter un nouvel espoir aux patients atteints de glioblastome afin qu’ils puissent récupérer après la chirurgie. Nous espérons que nous pourrons faire notre travail pour faire progresser cette technologie jusqu’à la clinique ».
L’approche thérapeutique pourrait également être appliquée à d’autres tumeurs solides agressives, comme le cancer du sein, connu pour ses récidives, car elle tire parti des macrophages dans les zones post-chirurgicales et permet de générer des macrophages spécifiques aux cellules résiduelles des cancers in situ, sans autre chirurgie invasive.
Sans compter que plus tôt cette année, la même équipe a mis au point un gel biodégradable améliorant également la capacité du système immunitaire à tenir le cancer à distance après l’ablation chirurgicale des tumeurs. Effectivement, le gel, testé sur des souris, libère des médicaments et des anticorps spéciaux qui, simultanément, épuisent les macrophages favorisant les cellules cancéreuses du site chirurgical, et activent les cellules T afin qu’elles puissent attaquer le cancer.
Face à ces découvertes, les auteurs concluent : « Cela donne de l’espoir pour prévenir la rechute du glioblastome. Nous prouvons qu’elles peuvent réellement éradiquer ces cellules souches de gliome, ce qui peut éventuellement empêcher le glioblastome de revenir. Nous pouvons améliorer considérablement la survie ».