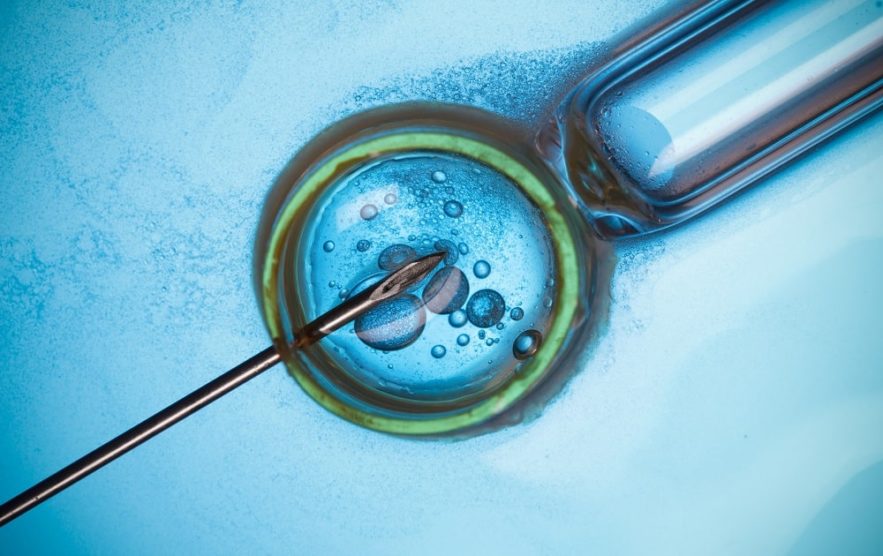
De nombreuses causes — cancers, exposition aux radiations, traitements médicaux, etc. — peuvent entraîner une infertilité partielle ou totale chez les hommes. Plusieurs techniques existent afin de traiter cette situation, la thérapie par cellules souches spermatogoniales (SSC) restant la plus prometteuse. Toutefois, jusqu’à présent, les résultats étaient incertains quant à la bonne différentiation des cellules souches. Récemment, une équipe de chercheurs a développé une méthode afin de s’assurer de la différentiation correcte des cellules souches en SSC.
L’infertilité affecte un homme sur sept en âge de procréer dans le monde. Une idée pour traiter la stérilité masculine est la thérapie par cellules souches spermatogoniales (SSC). Dans cette approche, les cellules souches de sperme dans les testicules sont transférées dans un tube à essai et cultivées pour devenir des spermatozoïdes à part entière. Cependant, un obstacle a été d’identifier les bonnes conditions pour que les SSC humains se développent en laboratoire.
Il y a eu de nombreuses tentatives, mais dans la plupart des cas, il n’était pas clair si les cellules cultivées étaient en fait des SSC. Des chercheurs de la faculté de médecine de l’Université de Californie à San Diego ont mis au point une méthode fiable de culture de cellules présentant les caractéristiques des SSC humaines. Leurs travaux ont été publiés dans la revus PNAS.
Assurer la bonne différenciation des cellules souches en SSC
Cette approche, qui s’appuie sur plusieurs techniques, y compris l’analyse de séquençage d’ARN unicellulaire, est une étape importante vers l’introduction de la thérapie SSC clinique, selon Miles Wilkinson, professeur au département d’obstétrique, de gynécologie et des sciences de la reproduction de la faculté de médecine de l’UC San Diego.
Les SSC permettent aux hommes de concevoir des enfants au-delà de 65 ans. Ces cellules spécialisées s’auto-renouvellent continuellement, produisant plus de SSC et se développant en spermatozoïdes de manière si prolifique que les hommes produisent plus de 1000 nouveaux spermatozoïdes toutes les quelques secondes.
Les progrès dans le domaine ont été entravés par le fait qu’il est extrêmement difficile de distinguer les SSC des autres cellules des testicules. Ce fut un grand pas en avant lorsque plusieurs laboratoires, dont l’équipe de Wilkinson, ont récemment utilisé une technique appelée séquençage d’ARN unicellulaire pour définir les caractéristiques moléculaires probables spécifiques aux SSC humaines.
Sur le même sujet : Découverte de nouvelles cellules souches capables de régénérer la structure osseuse
Inhibition de l’AKT : l’élément essentiel dans la différentiation en SSC
Dans son dernier effort, l’équipe de Wilkinson a utilisé ces informations de séquençage d’ARN unicellulaire pour purifier ce qu’elle pensait être des SSC humaines. En utilisant une méthode appelée transplantation de cellules germinales, elle a montré que les cellules purifiées étaient en effet très enrichies en SSC humaines. L’équipe a ensuite rassemblé le profil des gènes exprimés dans ces SSC humaines pour faire des suppositions quant aux conditions qui pourraient le mieux soutenir leur croissance en laboratoire.
En utilisant plus de 30 biopsies de testicules humains, les chercheurs ont déterminé les bonnes conditions nécessaires à la culture de cellules germinales immatures avec les caractéristiques des SSC. L’ingrédient clé était un inhibiteur de la voie AKT, un système cellulaire qui contrôle la division cellulaire et la survie. L’équipe de Wilkinson a déterminé que l’inhibition de l’AKT maintient les SSC humaines en inhibant le développement de précurseurs de sperme à un stade ultérieur. Plusieurs inhibiteurs de l’AKT sont actuellement utilisés pour traiter le cancer.
Avec cette approche, les chercheurs ont pu favoriser la culture de cellules humaines présentant les caractéristiques moléculaires des SSC pendant deux à quatre semaines. « Ensuite, notre objectif principal sera d’apprendre à maintenir et à stabiliser les SSC humaines plus longtemps afin qu’elles puissent être cliniquement utiles », conclut Wilkinson.